Plod, vývojové zpoždění nebo jiná patologie těhotenství.
Placenta je orgán, který se vytváří v místě implantace fetálního vajíčka do děložního endometria a který roste s plodem během těhotenství. Placenta má důležitou funkci při zásobování plodu kyslíkem a živinami. To se děje v důsledku cirkulace krve přes cévy pupeční šňůry, která se táhne od placenty k plodu plodu. Na druhé straně placenty jsou krevní cévy dělohy, které přinášejí všechny potřebné látky.
V důsledku toho dochází k přenosu živin k plodu placentou. Mělo by však být zřejmé, že krev matky je filtrována placentou, ale nemísí se s krví dítěte.
Placenta plní následující funkce:
- obohacuje fetální krev kyslíkem;
- odstraňuje oxid uhličitý z krve plodu;
- obohacuje fetální krev o živiny;
- odstraňuje produkty rozpadu z krve plodu.
Zdravá placenta roste během těhotenství, aby uspokojila rostoucí potřeby plodu. V době narození je jeho hmotnost asi 600 gramů. Pokud z nějakého důvodu dochází ke zpomalení růstu placenty, zmenšuje se objem krve, která k ní proudí, nebo se zmenšuje oblast kontaktu s dělohou ( jako při předčasném placentárním přerušení), pak je placentární nedostatečnost.
Placentární nedostatečnost se rozvíjí, když se placenta přestane vyrovnávat se svou funkcí a rozvíjí se stav nedostatku kyslíku a živin. Ve většině případů k této patologii dochází v důsledku poruch toku krve, které mohou být vyvolány matkami krve a krevních cév.
Příčiny placentární nedostatečnosti mohou být:
- arteriální hypertenze ( vysoký krevní tlak);
- některé léky;
- užívání drog ( zejména kokain, heroin, metamfetamin).
Placentární nedostatečnost je patologie, která přináší hlavní nebezpečí pro plod. V některých případech však může toto onemocnění ohrožovat život matky.
Placentární nedostatečnost je pro matku nebezpečná v následujících případech:
- Arteriální hypertenze. Vysoký krevní tlak, na jehož pozadí se vyvinula placentární nedostatečnost, je stav, který může ohrozit život matky. Na pozadí vysokého krevního tlaku může dojít k krvácení do mozku, prasknutí krevních cév a mnoha dalším nebezpečným následkům.
- Preeclampsia Přeeklampsie je patologický stav, který předchází eklampsii a která je formou pozdní toxikózy těhotenství. S touto patologií se zvyšuje krevní tlak, vyvíjí se periferní edém, v moči se objevuje nadbytek proteinů. Bez léčby může tento stav přejít do eklampsie, která je doprovázena křečemi a která může být léčena pouze vyloučením těhotenství.
- Předčasné oddělení normálně umístěné placenty. Placenta by měla odlupovat z děložní stěny až po narození plodu. Pokud k tomu dojde před dodáním, dojde k stavu známému jako předčasné oddělení normálně umístěné placenty. V tomto případě obvykle dochází k masivnímu krvácení z dělohy, což ohrožuje život matky a plodu.
Placentární nedostatečnost může způsobit následující patologie těhotenství:
- smrt plodu;
- hladovění kyslíkem při narození ( může způsobit poškození centrálního nervového systému);
- intrauterinní růstová retardace ( v těžkých případech - až 90% normy);
- podchlazení ( nízká tělesná teplota);
- hypoglykémie ( nízká hladina cukru v krvi);
- hypokalcemie ( nízký obsah vápníku v krvi);
- polycythemia ( nadměrné množství červených krvinek, čímž je krev viskóznější);
- předčasný porod;
- potřeba císařského řezu.
Placentární nedostatečnost může způsobit poškození následujících orgánů:
- mozek;
- gastrointestinální trakt.
Placentární nedostatečnost může být detekována následujícími způsoby:
- ultrazvuk ( Ultrazvukové vyšetření) a měření velikosti placenty a plodu;
- ultrazvuk a dopplerometrie krevního toku placenty;
- měření hladiny alfa-fetoproteinu v krvi matky;
- sledování stavu plodu.
Těhotenství je přirozený stav ženy, ale její normální průběh je prováděn složitými mechanismy, jejichž cílem je poskytnout plodu všechny životně důležité potřeby. Do toho jsou zapojeny dva funkční systémy - matka a placenta. Pokud je při práci těchto vzájemně propojených systémů nejméně jedna nejmenší porucha, mohou nastat dva patologické stavy - uteroplacentární a fetoplacentální nedostatečnost. To jsou úplně odlišné procesy, další věc je, že vedou ke stejné věci - k narušení krevního oběhu a výživy v systému matka-placenta-plod. Tento článek se zaměří na utero-placentární nedostatečnost.
1. Co je to uteroplacentální nedostatečnost během těhotenství
Toto je špatná cirkulace v systému matka-plod díky špatně vytvořenému vaskulárnímu systému v placentě.
Spojení plodu a matky se provádí pouze díky placentě. Začíná se formovat a rozvíjet od prvních dnů těhotenství, ale nelze jej považovat za nezávislé tělo. Role placenty je však obrovská, protože plod jí dostává kyslík a různé živiny. Hraje roli membrány a filtruje, brání mnoha chemikáliím proniknout do těla nenarozeného dítěte. V průběhu těhotenství hraje placenta roli endokrinního orgánu, produkuje řadu důležitých hormonů a látek nezbytných pro jeho zachování a normální průběh: progesteron, estrogen, choriový gonadotropin a další. Porušení funkce placenty je velmi nepříznivé pro těhotenství a vývoj plodu. .
2. Rizikové faktory
Děložně-placentární nedostatečnost má své příčiny:
Komplikace průběhu těhotenství: dlouhodobá a špatně léčitelná toxikóza, hrozba přerušení, potratu, nekompatibilita krve matky a plodu podle skupiny nebo Rhesus, nitroděložní infekce plodu, vícenásobné těhotenství atd.
Jakákoli chronická onemocnění matky: diabetes mellitus, srdeční vady (vrozené nebo získané), arteriální hypertenze, pyelonefritida, angína, anémie, autoimunitní onemocnění, nádory jakékoli lokalizace, včetně benigních atd.
Věk matky je starší 35 let a mladší 17 let.
Špatné životní podmínky.
Faktory prostředí: radiační a chemické účinky.
Špatné návyky: kouření, zneužívání alkoholu a drog.
Jakákoli akutní infekční onemocnění: ARVI, hepatitida atd.
Gynekologická onemocnění matky: kolpitida, adnexitida, myom, fibrom, menstruační dysfunkce atd.
Špatná porodnická anamnéza: jizva na těle dělohy, obvyklé nenesení, spontánní potraty, časté potraty, mrtvé narození, komplikovaný průběh předchozích narození a těhotenství atd.
3. Průběh uteroplacentální nedostatečnosti
Primární selhání se vyvíjí v časných stadiích těhotenství až do 12-14 týdnů, je to vzácné. Vyskytuje se v důsledku špatného připojení placenty k děložní stěně. S touto patologií je výživa embrya velmi rychle narušena a těhotenství zpravidla končí spontánním potratem nebo vývojem vrozených vrozených anomálií plodu.
Sekundární selhání se vyvíjí po 16 týdnech těhotenství a je častější. V tomto stavu je zpravidla hrozba potratu a žena skončí na patologickém oddělení.
4. Dojde k nedostatečnému toku děložního krevního oběhu: akutní a chronický
Akutní nedostatečnost je důsledkem náhlých poruch oběhu, v důsledku čehož může dojít k abrazi placenty, která často vede k úmrtí plodu a ukončení těhotenství.
Chronická nedostatečnost je nejčastějším narušením uteroplacentální cirkulace, v důsledku toho je narušena funkce placenty, plod nedostává vše potřebné a sám předčasně stárne.
Diagnóza nedostatečnosti uteroplacentální cirkulace v těhotenství je možná pouze pomocí dopplerografie (cévní vyšetření). A čím dříve bude studie dokončena, tím lépe. Pokud dojde ke změnám, lékař předepíše léčbu a mnoha problémům se lze vyhnout. Proto je vždy nutné provést všechna jmenování lékaře a v té době se zaregistrovat na prenatální klinice.
PŘEDNÁŠKA 4 PLACENTÁLNÍ NEDOSTATEČNOST A FETÁLNÍ RŮST ZPŮSOB SYNDROMPŘEDNÁŠKA 4 PLACENTÁLNÍ NEDOSTATEČNOST A FETÁLNÍ RŮST ZPŮSOB SYNDROM
Placentální nedostatečnost (PN)- klinický syndrom způsobený morfologickými a funkčními změnami placenty a porušením kompenzačně-adaptivních mechanismů, které poskytují normální růst a vývoj plodu, jakož i přizpůsobení ženského těla těhotenství. Placentární nedostatečnost je výsledkem komplexní reakce plodu a placenty na různé patologické stavy těla matky a projevuje se komplexem poruch transportních, trofických, endokrinních a metabolických funkcí placenty, které jsou základem patologie plodu a novorozence. Jeho klinickými projevy jsou syndrom zpomalení růstu plodu a / nebo hypoxie plodu. Syndrom fetální zpomalení růstu intrauterinní zpomalení růstu (FDVD); plod, který je malý na těhotenství, a plod s nízkou porodní hmotností jsou pojmy, které popisují plod, který nedosáhl svého růstového potenciálu v důsledku genetických nebo environmentálních faktorů. Společným kritériem je ztráta hmotnosti menší než 10. %opro gestační věk (tab. 12).
ICD-10
P00- poškození plodu a novorozence v důsledku stavu matky, které není spojeno s tímto těhotenstvím;
P01- poškození plodu a novorozence v důsledku těhotenských komplikací u matky;
P02- poškození plodu a novorozence v důsledku komplikací placenty, pupeční šňůry a fetálních membrán;
P05- pomalý růst a podvýživa plodu;
P20- intrauterinní hypoxie.
Placentární nedostatečnost je u těhotných žen často pozorována u porodnické a mimogenetické patologie a je 22,4-30,6%. Tudíž s hrozbou ukončení těhotenství je PN diagnostikována u více než 85% žen, s gestózou - u 30,3%, s arteriální hypertenzí - u 45%, s anémií a isoserologickou nekompatibilitou krve matky a plodu - až 32,2%, s myomem děloha -
Tabulka 12.10%oporodní hmotnost (g) v závislosti na pohlaví novorozence v jediném těhotenství
Gestační věk, týdny | Kluci | Dívky |
46%, s diabetem - 55%, se zhoršeným metabolismem tuků - u 24% těhotných žen. Perinatální úmrtnost u pacientů s PN dosahuje 40%, perinatální morbidita - 738-802 %o.Podíl hypoxicko-ischemického poškození centrálního nervového systému představuje 49,9%, což je 4,8krát vyšší než během nekomplikovaného těhotenství, u 11% novorozenců jsou zaznamenány respirační poruchy a aspirační syndrom a musí být provedena resuscitační opatření
15,2% dětí. Výskyt FWRS se liší v populaci od 10 do 23% dlouhodobých novorozenců v rozvinutých a rozvojových zemích. Frekvence SZRP se zvyšuje s klesajícím gestačním věkem. Přítomnost vrozených malformací, nitroděložní hypoxie, přechodných kardiorespiračních poruch, chromozomálních aberací, nitroděložních infekcí a také předčasně významně (až 60%) zvyšuje riziko perinatálních ztrát.
Perinatální úmrtnost mezi takovými novorozenci je významně vyšší než úmrtnost novorozenců s vhodnou termínovou hmotností (tabulka 13).
Tabulka 13.Perinatální úmrtnost ve FHW (na 1000)
G | 37-38 týdnů | 39-40 týdnů | 41-42 týdnů |
U novorozenců s celkovou hmotností 1 500–2500 g je tedy perinatální úmrtnost 5–30krát vyšší, váží méně než 1 500 g – 70–100krát vyšší než u novorozenců s normální tělesnou hmotností (Obr. 19).
70% plodů a novorozenců, jejichž váha není vyšší než 10% pro těhotenství, jsou malé kvůli ústavním faktorům (ženské pohlaví, mateřská příslušnost k určitým etnickým skupinám, parita narození, hmotnost a výškové vlastnosti matky), u těchto dětí se však míra perinatální úmrtnosti neliší. od dětí s normální hmotností. Mírná a těžká retardace růstu je stanovena hmotností 3 až 10% a méně než 3%.
Klasifikace.Neexistuje obecně přijímaná klasifikace PN v souvislosti s multifaktoriální etiologií. Podle toho strukturální jednotky vznikají patologickými procesy,existují tři formy placentární nedostatečnosti:
Hemodynamické projevy v uteroplacentálních a fetálně-placentárních zásobách;
Obr. devatenáct.Perinatální morbidita a úmrtnost u plodů a kojenců s nízkou porodní hmotností
Placentární membrána, charakterizovaná snížením schopnosti placentární membrány transportovat metabolity;
Buněčný parenchym, spojený s narušením buněčné aktivity trofoblastů a placenty.
Přidělte také hlavní- placentární nedostatečnost, ke které došlo před 16 týdny těhotenství, a - sekundárnívývoj později. Hlavníplacentární nedostatečnost se vyskytuje během implantace, rané embryogeneze a placentace pod vlivem různých faktorů (genetických, endokrinních, infekčních atd.) působících na gamety rodičů, zygota, blastocysta, formovaná placenta a sexuální aparát ženy jako celku. Primární fetoplacentální nedostatečnost se projevuje anatomickými změnami ve struktuře, umístění a připojení placenty, jakož i defekty vaskularizace a zhoršenou chorionickou maturací. Kromě toho se u této formy placentární nedostatečnosti častěji než v populaci detekují malformace plodu, chromozomální abnormality a nitroděložní infekce.
Sekundárnífetoplacentární nedostatečnost se vyvíjí pod vlivem exogenních faktorů a je pozorována ve druhé polovině těhotenství.
Placentární nedostatečnost (primární a sekundární) má ostrýnebo chronickýtok. OstrýPN vzniká v důsledku rozsáhlých placentárních infarktů a předčasného oddělení normálně lokalizované placenty s tvorbou retroplacentárního hematomu, což má za následek smrt plodu. ChronickýPN je pozorován u každé třetí těhotné skupiny s vysokým rizikem perinatální patologie. Chronická PN se vyvíjí brzy a pokračuje dlouhou dobu, a to v důsledku porušení kompenzačně-adaptivních mechanismů v kombinaci s oběhovými poruchami, mimovolně-dystrofickými změnami a zánětem nebo exacerbací spojenými s ženskou chorobou během těhotenství.
V současné době je vhodnější rozlišovat dekompenzované, subkompenzované a kompenzované formy. Tato klasifikace je založena na stupni retardace růstu plodu, přítomnosti a závažnosti příznaků chronické nitroděložní hypoxie plodu, stupni hemodynamických poruch v systému matka-placenta-plod, závažnosti porušení hormonální funkce placenty, účinnosti léčby.
Proces růstu plodu sestává ze tří po sobě jdoucích fází. První fáze - fáze buněčné hyperplázie trvá prvních 16 týdnů těhotenství. Druhá fáze - fáze simultánní hyperplázie a hypertrofie, což je současné zvýšení počtu buněk a zvětšení jejich velikosti, trvá období mezi 16. a 32. týdnem. Třetí fáze - hypertrofie buněk, trvá od 32. týdne před porodem a vyznačuje se rychlým nárůstem velikosti buněk. Při kvantitativním hodnocení rychlosti růstu plodu bylo zjištěno, že zvýšení hmotnosti plodu v jediné těhotenství o 5 g / den je zaznamenáno ve 14 až 15 týdnech, 10 g / den ve 20 týdnech, 30 až 35 g / den ve 32 až 34 týdnech. Následně se rychlost růstu tělesné hmotnosti snižuje. Klasifikace syndromu zpomalení růstu plodu je možná pouze při prodloužené ultrazvukové fetometrii během dynamického vyšetření těhotné ženy. Tvar rozlišuje: symetrický - s rovnoměrným zpožděním všech fetometrických ukazatelů (20-30% všech pozorování; asymetrický - převládající pokles velikosti břicha plodu (70-80%) a
smíšený - pokles všech fetometrických ukazatelů s převládajícím poklesem velikosti (obvodu) břicha plodu (5-10%). Podle závažnosti v předporodním období se rozlišuje I. stupeň - zpoždění fetometrických parametrů o 1–2 týdny od splatnosti za období těhotenství, II stupeň - zpoždění 2–4 týdny, III stupeň - zpoždění více než 4 týdny.
Etiologie a patogeneze.Vývoj placentární insuficience a SZRP závisí na porušení samotné placenty, přítomnosti somatické nebo porodnické patologie u matky, jakož i na stavu plodu. Reakce systému matka-placenta-plod závisí na každém z účastníků patologického procesu a na stupni narušení jejich kompenzačně adaptivních mechanismů. PN a SZRP se vyskytují u těhotných žen s vysokým rizikem rozvoje různých komplikací těhotenství.
S. Moddley (1997) identifikuje 3 hlavní skupiny příčin SZRP: mateřská, děložní, fetální:
1. Mateřský:
Demografické: věk, socioekonomický status, rasově-etnické charakteristiky;
Ústavní: genetické vlastnosti, výška, porodní hmotnost, hmotnost pacienta před těhotenstvím;
Nemoci: hypertenze, autoimunitní onemocnění, anémie, chronická kardiopulmonální onemocnění, chronická onemocnění ledvin, diabetes s vaskulárními změnami;
Trombofilní poruchy a mateřská hyperkoagulace;
Autoimunitní poruchy matky, včetně antifosfilipidového syndromu;
Nedostatečná výživa;
Ostatní: kouření, alkohol, drogy.
2. Děložní placenta:
Placentární infarkt;
Placentární moziacismus;
Abnormality dělohy;
Vícečetné těhotenství.
3. Ovoce:
Ústavní: genetické vlastnosti, pohlaví, postavení;
Aneuploidie / dědičné syndromy;
Intrauterinní infekce;
Anomálie plodu: vrozené malformace kardiovaskulárního systému, jediná pupeční tepna, feto-fetální transfuzní syndrom. Autor: A.T. Bunin (1993) rizikové faktory přispívající k rozvoji placentární nedostatečnosti a SZRP jsou:
Sociální a domácí (věk méně než 17 a více než 30 let, těhotenství mimo manželství, pracovní rizika, těžká fyzická práce, emoční stres, kouření, alkoholismus, drogová závislost, tělesná hmotnost menší než 50 kg);
Somatické (chronické specifické a nespecifické infekce, extragenitální choroby);
Porodnictví a gynekologie (infantilismus, menstruační dysfunkce, primární neplodnost, gynekologická onemocnění, spontánní potrat, nevyvíjející se těhotenství, komplikovaný průběh předchozího těhotenství a porodu);
Faktory spojené s tímto těhotenstvím (toxikóza v první a druhé polovině, hrozba ukončení těhotenství, vícenásobné těhotenství).
Mezi příčinami PN a SZRP zaujímá přední místo těhotenské komplikace (preeklampsie, hrozící potrat, potrat, isoserologická nekompatibilita mateřské a fetální krve, mnohočetné těhotenství) a extragenitální patologie (adrenální kortikální dysfunkce, hypertenze, chronická pyelonefritida, glomerulonefritida, diabetes mellitus). , kardiovaskulární a hematologická onemocnění matky).
Na začátku prvního trimestru těhotenství mají pacientky s vysokým rizikem vzniku placentární nedostatečnosti nižší invazi trofoblastu do myometrického segmentu spirálních tepen. Primárním spojením hemodynamických poruch u SZRP jsou změny v uteroplacentální cirkulaci (MPC), jejichž morfologickým základem je absence fyziologických gestačních změn ve spirálních tepnách a jejich křeči, jakož i poškození cévní stěny během autoimunitních procesů.
Vzhledem k patologickým změnám ve spirálových tepnách myometria, které zajišťují normální fungování uteroplacentálního oběhu, dochází k narušení krve
cirkulace v intervillousním prostoru. Zpomalení toku krve ve spirálních tepnách a intervillousním prostoru vždy vede ke snížení výměny plynů mezi krví matky a plodu. V důsledku poruch krevního oběhu v systému IPC se vyvíjí ischemický infarkt placenty, do kterého jsou zapojeny celé kotyledony. Na tomto pozadí je přirozeně také významně ovlivněn kapilární průtok krve v chorionických vilách.
Jedním z důležitých důvodů pro dysfunkci funkce placenty a rozvoj PN je nezralost vilusového stromu, která se projevuje změnami ve všech jejích strukturálních jednotkách. Působení škodlivých faktorů přispívajících k rozvoji placentární nedostatečnosti snižuje kompenzačně-adaptivní reakce v systému matka-placenta-plod.
Vedoucí roli určitých patogenetických mechanismů ve vývoji PN je do značné míry dána etiologickými faktory. V důsledku působení škodlivých faktorů v trimestru I-II (infekce, intoxikace) je vývoj PN způsoben hlavně převládající lézí placentární bariéry, zatímco jsou pozorovány nejzávažnější případy nezralosti klků s progresivní stromální sklerózou. Výrazně se snižuje průtok krve plodu a uvnitř placenty (v kapilárním loži placenty) s relativní bezpečností uteroplacentalu, což vede k rozvoji hypoxie plodu. V raných stádiích těhotenství (až 20–22 týdnů) s nedostatečně vyvinutými mechanismy fetální autoregulace (absolutní pokles počtu buněk v hyperplastické fázi růstu buněk) se vytvoří symetrická forma SZRP. Tato forma syndromu je charakterizována snížením všech fetometrických ukazatelů odrážejících růst plodu (biparietální velikost, obvod hlavy plodu, obvod a průměr břicha, velikost dlouhých tubulárních kostí, včetně stehenní kosti). Je třeba poznamenat, že frekvence SZRP s malformacemi je 19,5%. Na druhé straně jsou vrozené malformace u SZRP pozorovány u 7-15%. Asymetrická forma SZRP ve struktuře vrozených malformací je 30,6%, zatímco symetrická forma je 69,4%.
Ve druhé polovině těhotenství je hlavní patogenetickou vazbou u PN narušení toku uteroplacentální krve, což vede k chronické intrauterinní hypoxii plodu a tvorbě SZRP. Na pozadí chronického intrauterinního pokrytectví
jedná se o přerozdělení toku krve plodu, zaměřené primárně na normální fungování centrálního nervového systému. Hlavní tok arteriální krve jde do mozku plodu („Efekt šetřící mozek“).Klinicky se formuje asymetrická forma retardace růstu plodu, která se vyznačuje převládajícím poklesem obvodu břicha plodu. Existuje také tzv. Smíšená forma syndromu zpomalení růstu plodu, pozorovaná při těžké syndromové patologii plodu nebo se závažnou extagenitální patologií ženy doprovázené komplikovaným těhotenstvím (gestóza, prodloužené nebezpečí ukončení). Uvedená forma je charakterizována snížením všech fetometrických parametrů podle ultrazvukových dat s převládajícím poklesem velikosti břicha v důsledku výrazného nedostatečného vývoje podkožního tuku a objemu parenchymálních orgánů plodu. Pozorované změny jsou spojeny jak s narušením buněčných růstových procesů (syndromová patologie plodu), tak se závažnými, dlouhodobými hemodynamickými poruchami v systému matka-placenta-plod (extragenitální patologie matky, dlouhodobá gestóza, hrozící potraty).
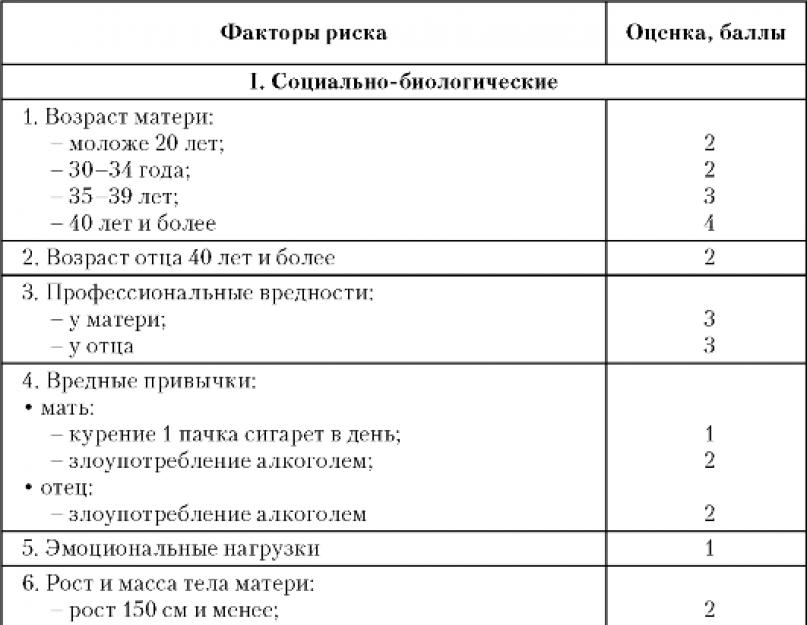
Diagnostika.V současnosti se k diagnostice placentární nedostatečnosti používají různé metody. Klinické metody zahrnují identifikaci anamnestických rizikových faktorů, objektivní vyšetření těhotné ženy a plodu měřením obvodu břicha a výšky děložního pozadí, stanovení tónu myometria, polohy plodu a výpočet jeho odhadované hmotnosti. Je známo, že zpoždění výšky postavení fundusu dělohy o 2 cm nebo více ve srovnání se správnou hodnotou pro specifické období těhotenství nebo absence zvýšení během 2 až 3 týdnů naznačuje pravděpodobnost vzniku syndromu zpomalení růstu plodu. Klinické hodnocení stavu jeho kardiovaskulárního systému se provádí pomocí auskultace. Přijatelný pro prenatální kliniky je systém pro stanovení rizika placentární nedostatečnosti, vyvinutý společností O.G. Frolova a E.N. Nikolaeva (1976, 1980), uvedená v tabulce. 14.
Důležitými informacemi při porodu o funkčních rezervách plodu je hodnocení kvality plodové vody. V současné době byla stanovena prognostická kritéria pro závažné komplikace placentární nedostatečnosti - meconiální aspirace u plodu a novorozence - podle povahy amniotické tekutiny v kombinaci s
Tabulka 14.Posouzení rizikových faktorů pro perinatální patologii
 Poznámka.Při skóre 10 nebo více existuje vysoké riziko perinatální patologie, 5-9 bodů znamená průměr, 4 nebo méně - nízký stupeň rizika.
Poznámka.Při skóre 10 nebo více existuje vysoké riziko perinatální patologie, 5-9 bodů znamená průměr, 4 nebo méně - nízký stupeň rizika.
údaje o jeho srdeční činnosti a respirační činnosti. Byla vytvořena bodová stupnice, která zohledňuje barvu vody, konzistenci meconia, gestační věk a přítomnost známek hypoxie podle hodnocení srdeční aktivity plodu. Při skóre 12 je pravděpodobnost aspirace meconia u plodu 50%, 15 nebo více - 100%. Významným omezením klinických diagnostických metod je individuální variabilita velikosti břicha a dělohy těhotné ženy, která závisí na antropometrických vlastnostech, závažnosti podkožní tukové vrstvy, množství plodové vody, poloze a počtu plodů. Změny v auskultačním obrazu se objevují pouze v pozdních stádiích fetálního utrpení a častěji se projevují již při porodu. Hodnocení stavu plodové vody v praxi je možné pouze po jejím propuštění, protože amnioskopie je neinformativní a amniocentéza je invazivní metoda, která má řadu omezení a vyžaduje zvláštní podmínky. U téměř 60% těhotných žen s klinickými metodami není placentární nedostatečnost detekována. Na druhé straně, u každé ze tří těhotných žen s podezřením na syndrom zpomalení růstu plodu, které jsou uvedeny na ultrazvuk, je potvrzena klinická diagnóza.
Laboratorní a instrumentální studia.S moderním komplexním vyšetřením těhotné ženy je nutné:
Identifikovat hlavní klinické projevy placentární nedostatečnosti, určit stupeň a formu SZRP, závažnost nitroděložní hypoxie;
Posoudit stupeň funkčních a morfologických změn v placentárním systému a jeho adaptivní schopnosti;
Stanovit etiologické faktory a patogenetické mechanismy rozvoje placentární nedostatečnosti, na jejichž základě zvolit optimální léčebnou možnost a vyvinout optimální porodnickou taktiku.
V tomto ohledu se stále více rozšiřují laboratorně-instrumentální diagnostické metody, které umožňují detekovat porušení v dřívějších fázích a včasně zahájit léčebná opatření.
Mezi laboratorní metody patří v posledních letech stanovení hormonálních a proteinových syntetických funkcí fetoplacentálního komplexu (placentární laktogen, progesteron, estriol,
kortizol, a-fetoprotein, SP1, PP12 atd.), biochemická studie jeho enzymatické aktivity (aspartátaminotransferáza, alanin aminotransferáza, alkalická fosfatáza atd.). Laboratorní diagnostika fetoplacentální nedostatečnosti, založená na stanovení hladin hormonů, má své charakteristické znaky, které jsou 2-3 týdny před klinickými projevy placentární nedostatečnosti. Fetoplacentální nedostatečnost v časném těhotenství závisí hlavně na nedostatečné hormonální aktivitě corpus luteum, doprovázené nízkými hladinami progesteronu a chorionického gonadotropinu. Později, v trimestrech těhotenství II a III, je vývoj PN doprovázen morfologickými poruchami, které postupně vedou k rozvoji nedostatečnosti hormonálně produkující funkce placenty.
Časným předklinickým příznakem placentární nedostatečnosti je snížení syntézy všech hormonů fetoplacentálního systému (estrogen, progesteron, placentární laktogen), proto dynamické stanovení hormonů s optimální detekcí včasné placentární nedostatečnosti je časná data těhotenství a před narozením. Nejúplnější informace o stavu plodu lze získat integrovaným stanovením několika hormonů. Klinický význam stanovení placentárního laktogenu (PL) v krevním séru těhotných žen je způsoben skutečností, že jeho koncentrace pod 4 μg / ml naznačuje dysfunkci placenty v patologicky probíhajícím těhotenství a je prognostickým příznakem narušení funkčního stavu plodu. Při hrozícím potratu je snížení koncentrace PL nejčasnějším diagnostickým ukazatelem nepříznivého těhotenského výsledku. V případě intrauterinní fetální smrti klesá koncentrace PL mnohem dříve než ukončení srdečního rytmu plodu. Pokles PL o 50% nebo více z průměrné úrovně naznačuje kritické snížení funkce placenty a porušení plodu. Když ponorka klesne o 80%, dojde k prenatální fetální smrti. Diagnostickou hodnotou je porovnání koncentrace PL v krvi a plodové vodě. Poměr koncentrace hormonu v krvi k jeho hladině v plodové vodě je obvykle od 9: 1 do 14: 1. Při mírné placentární nedostatečnosti klesá na 6: 1, s těžkými - méně než 6: 1. Ve druhé polovině těhotenství je obsah progestivního
rona je indikátorem hormonální funkce placenty. S placentární nedostatečností klesá koncentrace progesteronu v závislosti na jeho závažnosti o 30-80%. Na druhou stranu, s řadou těhotenských komplikací, kdy dochází k patologickému zvýšení hmotnosti placenty, se zvyšuje produkce progesteronu. Vysoká hladina progesteronu je tedy pozorována u těhotných žen s Rh senzibilizací, při těžkých formách diabetu a při selhání ledvin, když je narušena hormonální exkrece z krve. V těchto případech znamená zvýšená koncentrace progesteronu nepříznivou prognózu průběhu těhotenství.
Definice estriolu jako metody monitorování stavu plodu během těhotenství získala největší praktický význam. Při komplikovaném těhotenství je snížení hladiny estriolu časným diagnostickým příznakem zhoršeného vývoje plodu. Snížení vylučování estriolu močí na 12 mg / den nebo méně naznačuje výrazné zhoršení plodu a fetoplacentálního systému. Významné fluktuace tohoto ukazatele v normě as podvýživou plodu vyžadují provedení studií dynamiky. Příznakem placentární nedostatečnosti je snížení hladiny estriolu v plodové vodě. Pro diagnózu placentární nedostatečnosti se stanoví index estriolu - poměr množství hormonu v krevní plazmě a moči. Postupem selhání se index snižuje. Jednou z nejčastějších příčin nízkého estriolu u těhotných žen je retardace růstu plodu. Prudký pokles estriolu (méně než 2 mg / den) je pozorován u anencefálie plodu, hypoplasie jeho nadledvinek, Downova syndromu, intrauterinní infekce (toxoplasmóza, zarděnka, cytomegalovirová infekce). Vysoká hladina estriolu je pozorována při vícenásobném těhotenství nebo u velkého plodu. Kromě stavu plodu existuje celá řada exogenních a endogenních faktorů, které ovlivňují biosyntézu, metabolismus a vylučování estriolu. Léčba těhotné ženy kortikosteroidy tedy způsobuje dočasné potlačení funkce nadledvinek plodu, což vede ke snížení hladiny estriolu. Při léčbě glukokortikoidy nebo antibiotiky těhotné ženy se také snižuje syntéza estriolu. Těžká onemocnění jater u matky mohou vést k narušení konjugace estrogenů a jejich eliminaci žlučí. Změna funkce ledvin u těhotné ženy vede ke snížení clearance
ol, v důsledku čehož se obsah hormonů v moči snižuje, jeho hladina v krvi nepřiměřeně stoupá k plodu. Ve vzácnějších případech se vyskytují vrozené enzymatické defekty placenty, které mohou způsobit extrémně nízké hodnoty estriolu, zatímco plod nebude narušen. Podobné vzorce jsou pozorovány při stanovení obsahu estriolu v krvi těhotných žen. Zvláště zajímavé je studium hladiny neuronově specifické enolázy v krvi matky a izoenzym kreatin kinázy v plodové vodě jako předporodní markery zhoršeného vývoje mozku, jejichž hladina se zvyšuje s hypoxií plodu. Je třeba mít na paměti, že většina hormonálních a biochemických testů má široké hranice jednotlivých vibrací a nízkou specificitu, aby bylo možné získat spolehlivá data, je nutné určit úroveň hormonu nebo enzymu v dynamice. Společnou nevýhodou těchto testů je nedostatečná interpretace výsledku v době studie plodu.
Uvedené nevýhody jsou zbaveny metod ultrazvuku a funkčního hodnocení plodu (kardiotocografie, kardiointervalografie, Dopplerometrická analýza průtoku krve), které v současné době vedou k diagnostice placentární nedostatečnosti. Hlavní význam sonografiepro diagnostiku placentární nedostatečnosti je identifikovat syndrom retardace růstu plodu a určit jeho tvar a závažnost. Ultrazvuková diagnóza retardace růstu plodu je založena na srovnání fetometrických indikátorů získaných na základě studie s normativními indikátory pro daný gestační věk. Nejrozšířenější v diagnostice intrauterinní retardace růstu bylo měření velikosti hlavice biparietální, průměrných průměrů hrudníku a břicha, jejich obvodů a ploch průřezu, jakož i délky femuru. Pro kontrolu vývoje plodu se používá percentilní přístup, který umožňuje každému přesnému gestačnímu věku přesně určit shodu velikosti plodu s gestačním věkem a také míru, do jaké se odchylují od standardních hodnot. Diagnóza szrp se provádí, pokud je velikost plodu pod 10 %onebo více než dvě standardní odchylky pod průměrem pro daný gestační věk. Na základě výsledků ultrazvuku můžete
určit formy SZRP (symetrické, asymetrické), které se vyznačují různými poměry ukazatelů fetometrie (délka stehna / břicho, délka stehna / obvod hlavy). Možná vytvoření „smíšené“ formy retardace intrauterinního růstu. Vyznačuje se nepřiměřeným zpožděním všech ukazatelů fetometrie s nejvýraznějším zpožděním ve velikosti břicha. Na základě údajů o fetometrii lze určit závažnost retardace růstu plodu. Na I. stupni je rozdíl mezi fetometrií a normativními indikátory a jejich soulad s ukazateli typickými pro těhotenství o 2 týdny kratší (34,2%), s II stupně - o 3-4 týdny kratší (56,6%), s III - kratší období o více než 4 týdny (9,2%). Závažnost nitroděložní retardace růstu koreluje se závažností placentární nedostatečnosti a nepříznivých perinatálních výsledků.
R. Deter a kol. (1995) navrhl novou upravenou stupnici hodnocení novorozeneckého vývoje (NGAS- Neonatální Gřádek Asessessment Sjádro). Je založen na výpočtech indexů realizace potenciálního růstu. (GRPI- Gřádek Pdůkazní Realizace Jándex). Tyto indexy lze použít pro takové fetometrické parametry, jako je hmotnost, obvod hlavy, břicho a stehna, jakož i růst plodu. Stupnice je založena na srovnávacím posouzení údajů získaných v trimestru II těhotenství pomocí ultrazvuku a údajů při narození. Vyhodnocuje shodu geneticky stanoveného potenciálu růstu hmoty plodu a údajů získaných při narození. S jeho pomocí je možné posoudit, zda novorozenec má zpoždění v antropometrických ukazatelích nebo zda je plně využit jeho potenciál hromadného růstu. Měřítko lze použít nejen pro SZRP, ale také pro vícenásobné těhotenství, jakož i pro hodnocení velkých plodů.
V poslední době se echografická studie také používá k posouzení stavu pupeční šňůry jako kritéria pro nitroděložní utrpení plodu. Pokud průměr pupeční šňůry během těhotenství 28-41 týdnů není větší než 15 mm (hubená pupeční šňůra) a průměr žil a tepen je 8 mm, respektive 4 mm, 66% případů má příznaky hypoxie plodu a 48% má syndrom zpomalení růstu plodu. Dalším kritériem nitroděložního utrpení plodu a prognostickým příznakem trápení novorozence jsou autoři přesvědčeni, že šňůra je příliš rozvinutá.
Důležitou informací o stavu plodu je jeho motorická a respirační aktivita. Přítomnost pravidelně se opakujících respiračních pohybů plodu v přítomnosti meconia v plodové vodě je rizikovým faktorem pro vývoj aspiračního syndromu. Obzvláště nepříznivým prognostickým faktorem je dlouhé období pohybu typu "Dýchání"(udušení).
V posledním desetiletí se používal k provádění fetometrie, včetně placentární nedostatečnosti a SZRP trojrozměrný ultrazvuk.Tato technika má větší přesnost při měření průměru biparieta, obvodu hlavy a obvodu břicha plodu, délky stehenní kosti ve srovnání s dvourozměrným ultrazvukem, zejména s nízkou vodou nebo nesprávnou polohou plodu v děloze. To dává významně menší chybu ve výpočtu odhadované tělesné hmotnosti plodu (6,2-6,7% oproti 20,8% u dvojrozměrného ultrazvuku).
V diagnostice placentární nedostatečnosti hraje důležitou roli ultrazvuková placentografie,což kromě určení lokalizace placenty umožňuje vyhodnotit její strukturu a velikost. Výskyt fáze II až 32 týdnů a fáze III placentární zralosti až 36 týdnů těhotenství naznačuje její předčasné zrání. V některých případech se pomocí ultrazvuku pozoruje cystická změna placenty. Placentární cysty jsou definovány jako echo-negativní formace různých tvarů a velikostí. Vyskytují se častěji na fetální straně placenty a jsou vytvářeny v důsledku krvácení, změkčení, srdečních záchvatů a jiných degenerativních změn. V závislosti na patologii těhotenství se nedostatečnost funkce placenty projevuje snížením nebo zvětšením tloušťky placenty. Tak, typické pro gestózu, hrozbu ukončení těhotenství, SZRP „tenká“ placenta (až 20 mm v III. Trimestru těhotenství). U hemolytických onemocnění a diabetes mellitus je placentární nedostatečnost indikována „tlustou“ placentou (do 50 mm nebo více). Jednou z nejrozšířenějších metod funkčního hodnocení stavu plodu je kardiotocografie.Spolu s indikátory fetální srdeční aktivity vám tato metoda umožňuje zaregistrovat motorickou aktivitu plodu a kontraktilní aktivitu dělohy. Nejčastěji používaný nestresový test, který hodnotí povahu srdeční aktivity plodu in vivo. Méně obvyklá reakce plodu na určité „vnější“ vlivy (zvuk,
děložní kontrakce pod vlivem exogenního oxytocinu atd.). V případě syndromu zpomalení růstu plodu odhaluje nestresový test fetální tachykardii ve 12% případů, snížení variability bazálního rytmu o 28%, variabilní zpomalení o 28% a pozdní zpomalení o 13%. Současně je třeba mít na paměti, že vzhledem k načasování tvorby reflexu myokardu (do 32. týdne těhotenství) je vizuální hodnocení kardiotogramů možné pouze ve třetím trimestru těhotenství. Kromě toho, jak ukazují výsledky odborných hodnocení, četnost nesrovnalostí ve vizuálním hodnocení kardiotogramů několika specialisty může dosáhnout 37–78%. Povaha kardiotocografické křivky závisí nejen na gestačním věku, ale také na pohlaví plodu, tělesné hmotnosti a zvláštnostech řízení práce (analgezie, stimulace práce, antikoncepce). V posledních letech se definice echografické studie tzv. Biofyzikálního profilu plodu velmi rozšířila (tabulka 15). Tento test zahrnuje komplexní skóre (stupnice od 0 do 2 bodů) množství plodové vody, fyzické aktivity a svalového tónu plodu, respiračních pohybů, jakož i výsledky nestresového kardiotocografického testu.
8-10 bodů označuje normální stav plodu. Opakovaný výzkum by měl být prováděn pouze u těhotných žen s vysokým rizikem po 1-2 týdnech. Při hodnocení 4–6 bodů se určuje porodnická taktika s přihlédnutím ke známkám fetální dospělosti a připravenosti porodního kanálu. V případě nedostatečné zralosti plodu a nedostatečné připravenosti porodního kanálu se studie opakuje po 24 hodinách. Pokud se dosáhne opakovaného nepříznivého výsledku, měla by být kortikosteroidová terapie následována porodem nejdříve po 48 hodinách. Skóre 0-2 bodů je známkou naléhavého a pečlivého doručení. Pokud neexistují známky plodové zralosti, mělo by být porod provedeno po 48hodinové přípravě těhotné ženy s kortikosteroidy.
Parametr | Body |
|
Plodová voda | Amniotická tekutina je vizualizována ve většině děložních dutin. Největší vertikální velikost volné části vody přesahuje 1 cm | Amniotická tekutina není ve většině děložních dutin vizualizována. Největší vertikální velikost volné části vody nepřesahuje 1 cm |
Fetální motorická aktivita | Přítomnost nejméně tří samostatných pohybů těla plodu do 30 minut od pozorování | Přítomnost dvou samostatných pohybů těla plodu nebo méně do 30 minut od pozorování |
Fetální dechové pohyby | Registrace alespoň jedné epizody respiračních pohybů plodu během 30 minut, která trvá 30 sekund nebo více | Absence fetálních respiračních pohybů nebo registrace epizody respiračních pohybů trvajících méně než 30 s po dobu 30 minut |
Svalový tón plodu | Končetiny plodu jsou ve flexi, kmen je mírně ohnutý; fetální hlava je přitisknuta k hrudi. Po pohybu se plod vrátí do své původní polohy | Končetiny a kmen plodu jsou částečně nebo úplně nataženy, ruka je otevřená. Po pohybu se plod nevrátí do stavu flexe |
Nestresový test | Přítomnost dvou zrychlení nebo více s amplitudou nejméně 15 úderů a trváním alespoň 15 s po dobu 40 minut studia | Přítomnost méně než dvou zrychlení s amplitudou nejméně 15 úderů a dobou trvání alespoň 15 s po dobu 40 minut studia |
pouze o tvorbě děložního placentárního a fetálně placentárního oběhu, ale také odhaluje hemodynamické markery chromozomální patologie. Intraplacentální cirkulace (průtok krve ve spirálních tepnách a terminálních větvích pupeční tepny) u nekomplikovaného těhotenství je charakterizována progresivním poklesem vaskulárního odporu, který odráží hlavní stádia placentární morfogeneze. Nejvýraznější pokles vaskulárního odporu ve spirálních tepnách v období 13-15 týdnů a v terminálních větvích pupeční tepny - za 24-26 týdnů, což je 3-4 týdny před maximálním poklesem vaskulárního odporu v děložních tepnách a terminálních větvích pupeční tepny. Ve studii průtoku krve v děložních tepnách, umbilikálních tepnách a intra-placentárním oběhu je zásadně důležité předpovídat vývoj gestózy a placentární nedostatečnosti, počínaje 14-16 týdny těhotenství, což je skutečnost, že porušení intraplacentálního krevního toku je detekováno o 3-4 týdny dříve než v hlavních souvislostech.
Nejvýznamnější studie děložně-placentární a fetální-placentární cirkulace za účelem předvídání vývoje a včasné diagnostiky gestózy a placentární nedostatečnosti se stává v II. Trimestru těhotenství. Kromě zvýšení indexů vaskulární rezistence v děložních tepnách jsou možné také dikrotické záchvaty v časné diastolové fázi. Pokud jsou v systému matka-placenta-plod identifikovány patologické hemodynamické ukazatele, jsou pacienti vystaveni vysokému riziku vývoje gestózy a fetoplacentální nedostatečnosti a potřebují diferencovanou lékařskou opravu odhalených hemodynamických poruch. V případě porušení v uteroplacentálním krevním oběhu jsou léky volby léky, které zlepšují reologické vlastnosti krve (pentoxifylin, kyselina acetylsalicylová), a v případě porušení vazby plodu a placenty je vhodné použít hemoderivát. V převážné většině případů komplikovaného těhotenství a mimoděložních onemocnění je počátečním stadiem vývoje patologického procesu narušení toku uteroplacentálního krevního oběhu s postupným zapojením fetálně placentárního krevního oběhu a kardiovaskulárního systému plodu. Uvedená sekvence patogenetických mechanismů pro vývoj hemodynamických poruch
prezentováno ve vývoji A.N. Strizhakov a kol. (1986) klasifikace poruch toku krve v systému matka-placentaplod:
IA stupeň - narušení toku uteroplacentální krve intaktním fetálně placentálním;
IB stupeň - narušený průtok krve plodu-plodu s intaktním uteroplacentálem;
II. Stupeň - současné porušení uteroplacentálního a fetálně-placentárního krevního toku, nedosažení kritických hodnot (zachování pozitivně orientovaného diastolického krevního toku v pupeční tepně);
III. Stupeň - kritické narušení fetálně-placentárního krevního toku (absence nebo retrográdní směr end-diastolického krevního toku) se zachovaným nebo narušeným uteroplacentálním krevním tokem.
Snížení rychlosti průtoku krve v pupeční tepně k diastole na nulu nebo výskyt retrográdního průtoku krve ukazuje na významné zvýšení vaskulární rezistence v placentě, která je obvykle kombinována s kriticky vysokou úrovní akumulace laktátu, hyperkapnie, hypoxémie a acidémie u plodu.
V komplexní studii arteriálního oběhu plodu s nejčastější komplikací těhotenství - placentární nedostatečnost - jsou zaznamenány následující změny:
Zvýšené indexy vaskulárního odporu v pupeční tepně (LMS více než 3,0);
Indexy zvýšené vaskulární rezistence v aortě plodu
(LMS více než 8,0);
Indexy snížené vaskulární rezistence ve střední mozkové tepně (LMS méně než 2,8);
Snížený průtok krve v renálních tepnách;
Porušení intrakardiální hemodynamiky (výskyt zpětného toku krve trikuspidální chlopní).
S fetoplacentální nedostatečností je narušena intrakardiální hemodynamika plodu, která spočívá ve změně poměru maximálních rychlostí průtoku krve ventily ve prospěch levého srdce, jakož i v přítomnosti regurgitačního toku trikuspidální chlopní. V kritickém stavu plodu jsou odhaleny následující změny fetální hemodynamiky:
Nulový nebo negativní průtok krve v pupeční tepně;
Regurgitace trikuspidální chlopní;
Nepřítomnost diastolické složky průtoku krve v aortě plodu;
Zvýšená diastolická složka toku krve ve střední mozkové tepně;
Porušení průtoku krve v žilním kanálu a spodní vena cava, zatímco dopplerometrickým kritériem pro zhoršený průtok krve v žilním kanálu je snížení rychlosti průtoku krve v pozdní diastolové fázi, až na nulové nebo záporné hodnoty. V kritickém stavu plodu pulsační index v žilním kanálu překračuje 0,7. Dopplerometrická kritéria pro zhoršený průtok krve v dolní duté žíle jsou zvýšení rychlosti zpětného toku krve o více než 27,5-29% a výskyt nulového nebo reverzního průtoku krve mezi systolickým a časným diastolickým tokem.
Diferenciální diagnostika.Byla navržena řada kritérií, která umožňují diferenciální diagnostiku mezi syndromem retardace růstu plodu s konstitučně malým plodem („plod malý pro těhotenství“). Některá kritéria použitá při hodnocení stavu plodu, zatímco jiná - novorozenci.
1. Hodnocení trendu růstu plodu na základě vypočtených ukazatelů realizace potenciálního růstu (GRPI- Gřádek Pdůkazní Realizace Jándex). Tyto indexy lze použít pro takové fetometrické parametry, jako je hmotnost, obvod hlavy, břicho a stehna, jakož i růst plodu. Stupnice je založena na srovnávacím posouzení údajů získaných v trimestru II těhotenství pomocí ultrazvuku a údajů při narození.
2. Použití souboru indikátorů v diagnostice SZRP (výpočet odhadované hmotnosti plodu, odhad množství plodové vody, přítomnost hypertenze v matce) může zlepšit přesnost diagnostiky SZRP na 85%.
3. Dopplerovské studium toku krve v pupečních a děložních tepnách.
4. Výpočet indexu ponderalu
Ponderální index \u003d hmotnost vg? 100 / délka v cm? 3.
5. Zvýšení počtu jaderných forem červených krvinek v krvi plodu získané kordocentezí (v důsledku hypoxie v přítomnosti
PN a SZRP).
6. Vlastnosti přírůstku tělesné hmotnosti po narození (25% novorozenců se závažným (III) stupněm SZRP do 24 měsíců života zůstává za indexy růstu hmotnosti pod 3) %o).
Rutina prenatální screeningpro diagnostiku placentární nedostatečnosti a výsledné SZRP zahrnuje:
Identifikace těhotných vysoce rizikových skupin PN a SZRP;
Hodnocení výšky děložního pozadí během těhotenství;
Biochemický screening (dvojité a trojité testy); podrobné ultrazvukové vyšetření za 10-14 týdnů, 20-24 týdnů,
30-34 týdnů těhotenství s hodnocením anatomie plodu, identifikace markerů chromozomálních abnormalit, intrauterinní infekce, malformací plodu;
Ultrazvuková fetometrie v uvedeném čase s diagnózou SZRP symetrické a asymetrické formy, hodnocení závažnosti syndromu;
Odhad množství plodové vody;
Posouzení stupně zralosti placenty;
Dopplerometrie průtoku krve v děloze, spirálních tepnách, pupeční tepně a jejích terminálních větvích po 16-19 týdnech, 24-28 týdnech, 32-36 týdnech těhotenství;
Posouzení fetální hemodynamiky (střední mozková tepna, aorta, renální tepny, žilní kanál, dolní dutá vena);
Kardiotocografie (po dobu více než 28 týdnů těhotenství).
Kromě toho lze podle indikací použít invazivní výzkumné metody (amniocentéza, biopsie choriových klků, placentcentéza, kordocentéza), následované karyotypizací s vysokým rizikem výskytu chromozomálních abnormalit a genových defektů u plodu.
Mezi preventivní opatřeníměl by uvádět:
Léčba mimoděložních chorob před těhotenstvím;
Korekce metabolických poruch a krevního tlaku od počátku těhotenství;
Dodržování racionální stravy a režimu těhotné ženy;
Jmenování protidestičkových látek (kyselina acetylsalicylová - 100 mg / den, dipyridamol - 75 mg / den, pentoxifylin - 300 mg / den) a antikoagulanty (NMH);
Použití deprotienizovaného hemoderivátu (200 mg 3krát denně, 21-30 dní);
Použití gestagenů (dydrogesteronu, mikronizovaného progesteronu) u těhotných žen s obvyklou ztrátou těhotenství od časného těhotenství;
Jmenování multivitaminových komplexů.
TerapiePN a SZRP by se měly zaměřit na: zlepšení děložního a fetálního placentárního průtoku krve; intenzifikace výměny plynu; korekce reologických a koagulačních vlastností krve; eliminace hypovolémie a hypoproteinémie; normalizace vaskulárního tónu a kontraktilní aktivity dělohy; zvýšená antioxidační ochrana; optimalizace metabolických a metabolických procesů.
Indikace pro hospitalizaci.Subkompenzovaná a dekompenzovaná PN, kombinace PN a SZRP s extragenitální patologií, gestóza, ohrožení předčasného porodu.
Léčba drogy.Vzhledem k tomu, že mezi příčinami placentární nedostatečnosti, škodlivých účinků chemických látek, nevyvážené stravy, mimogenních a infekčních nemocí, gestózy, dlouhodobé hrozby ukončení těhotenství a dalších těhotenských komplikací, je velmi důležité, je metodicky správné zahájit léčbu PN s vyloučením nepříznivých účinků těchto etiologických faktorů. Normalizace stravy ve skupině těhotných žen s nízkou životní úrovní v důsledku zvýšení obsahu bílkovin a základních minerálů při současném snížení podílu tuků a uhlohydrátů na vyváženou úroveň umožňuje snížit výskyt SZRP o 19%.
Při léčbě fetoplacentální insuficience je velmi důležitá normalizace děložního tonusu, protože jeho zvýšení přispívá k poruchám oběhu v intervillousním prostoru v důsledku snížení venózního výtoku. K tomuto účelu se používají antispasmodická léčiva a tocolytika (fenoterol, hexoprenalin). Jak ukázaly naše studie, s adekvátní léčbou PN na pozadí hrozby ukončení těhotenství v 90% případů je možné dosáhnout pozitivního účinku. Účinnost léčby kompenzovaných a subkompenzovaných forem placentární nedostatečnosti u těhotných žen s anémií se blíží 100%. Je také docela účinný při léčbě PN s použitím antibakteriálních léků na
nitroděložní infekce (pozitivní účinek v 71,4% případů). Současně je u těhotných žen s gestózou léčba placentární nedostatečnosti účinná pouze u 28,1% s počátečním oběhovým onemocněním v systému matka-placenta-plod, což je pravděpodobně způsobeno morfologickými poruchami v procesu tvorby placenty.
Nejběžnějšími léky v léčbě placentární nedostatečnosti jsou antiagregační látky a antikoagulancia. Z této skupiny léčiv se obvykle používá kyselina acetylsalicylová, dipyridamol, pentoxifylin, nikospan, xantinol, heparin. Snížení projevů placentární nedostatečnosti během léčby antiagregačními činidly a antikoagulanty je způsobeno zvýšenou aktivitou periferních cytotrofoblastů, snížením objemu intervilních fibrinoidů, lepených klků, krvácení do mezivalu a placentárním infarktem. Použití protidestičkových látek je nejúčinnější v případě nadměrné aktivace vazebně-destičkové vazby hemostázového systému, u závažnějších poruch, které zahrnují také patologické zesílení plazmatické vazby, je vhodné doplnit o léčbu heparinem. Tento lék má antihypoxický účinek, podílí se na regulaci tkáňové hemostázy a enzymatických procesů. Heparin neproniká placentární bariérou a nemá škodlivý účinek na plod. V posledních letech byly při léčbě placentární nedostatečnosti použity NMH, které mají výraznější antitrombotickou aktivitu a vykazují méně vedlejších účinků.
Vzhledem k vztahu mezi ukazateli děložního průtoku krve a aktivitou krevních enzymů u těhotných žen s vysokým rizikem perinatální patologie je vhodné pro prevenci a léčbu fetální hypoxie provádět metabolickou terapii pomocí ATP, drogy inosinu-F, kokarboxylázy, vitamínů a antioxidantů. Metabolická terapie je nezbytnou součástí léčby PN, protože snižuje intenzitu peroxidace lipidů. Ke stabilizaci strukturních a funkčních vlastností buněčných membrán, ke zlepšení trofismu plodu se používají membránové stabilizátory - vitamin E a esenciální látky. V současné době zahrnuje metabolická terapie fetoplacentální nedostatečnosti v ambulantních i lůžkových zařízeních použití vysoce purifikovaného
telecí hemoderivát s peptidy s nízkou molekulovou hmotností a deriváty nukleových kyselin. Základem farmakologického působení je účinek na procesy intracelulárního metabolismu, zlepšení transportu glukózy a absorpce kyslíku v tkáních. Začlenění velkého množství kyslíku do buňky vede k aktivaci procesů aerobní glykolýzy, ke zvýšení energetického potenciálu buňky. Při léčbě PN aktivuje aktovegin buněčný metabolismus zvýšením transportu, akumulací a zvýšením intracelulárního využití glukózy a kyslíku. Tyto procesy vedou ke zrychlení metabolismu ATP a ke zvýšení energetických zdrojů buněk. Sekundárním efektem je zvýšené zásobování krví. Základem antiischemického účinku Actoveginu je také antioxidační účinek (aktivace enzymu superoxiddismutázy). Actovegin se používá jako intravenózní infuze 80-200 mg (2-5 ml) ve 200 ml 5% roztoku glukózy (~ 10) nebo v dražé (1 tableta 3x denně po dobu 3 týdnů). Neurochranný účinek Actoveginu ve vztahu k mozku plodu pod hypoxií byl prokázán. Má také anabolický účinek, který hraje pozitivní roli.
s SZRP.
U subkompenzovaných a dekompenzovaných forem PN je také možné kombinované použití aktoveginu a instenonu, kombinovaného léčiva, které kombinuje nootropické, vaskulární a neurotonické složky.
Adekvátní přísun kyslíku plodu hraje velkou roli při jeho podpoře života. V tomto ohledu je pro PN indikována kyslíková terapie, je však třeba vzít v úvahu vývoj ochranných reakcí při inhalaci nad 100% kyslíku, proto se používá 30 až 60 minutových inhalací plynné směsi s koncentrací kyslíku nejvýše 50%.
Důležitou součástí léčby PN na pozadí extragenitální patologie a těhotenských komplikací je infuzní terapie. Jednou z nejdůležitějších složek komplexu terapeutických opatření pro placentární nedostatečnost je zajištění energetické energie plodu zavedením glukózy ve formě intravenózních infuzí v kombinaci s odpovídajícím množstvím inzulínu.
Infuze směsi glucosonokainu jako prostředku ke snížení vaskulárního spasmu neztratila terapeutickou hodnotu,
zlepšit mikrocirkulaci a průtok krve v arteriálních cévách placenty. Intravenózní podání ozonizovaného izotonického roztoku chloridu sodného přispívá k normalizaci plodu v přítomnosti laboratorních a instrumentálních známek hypoxie.
Za účelem korekce hypovolémie, zlepšení reologických vlastností krve a mikrocirkulace v placentě je účinné zavedení reopoliglucinu a roztoků na bázi hydroxyethylovaného škrobu. Infuze 10% roztoku hydroxyethylovaného škrobu při léčbě PN na pozadí gestózy může dosáhnout významného snížení ukazatelů vaskulární rezistence v děložních tepnách a perinatální úmrtnost klesá ze 14 na 4%. Pokud je u těhotných žen zjištěna hypoproteinémie a existuje-li abnormalita v plazmovém spojení hemostázového systému, provede se infuze čerstvě zmrazené plazmy v množství 100-200 ml 2-3krát týdně. V případě nedostatku bílkovin, výrazné ztráty nebo zvýšené potřeby proteinů, zejména s SZRP, je možné použít infuzní terapii léky obsahujícími roztok aminokyseliny (aminosol L-800, aminosteryl KE 10% bez uhlohydrátů, infezol 40). Je třeba mít na paměti, že zvýšení koncentrace aminokyselin v mateřské krvi nevede vždy ke zvýšení jejich obsahu v plodu.
Kromě toho jsou při léčbě AF velmi důležité fyzikální metody vlivu (elektrolytická relaxace dělohy, elektroforéza hořčíku, jmenování tepelných procedur v perinefrické oblasti), které uvolňují myometrium a vedou k vazodilataci.
Nová metoda v léčbě těhotných žen s PN vede terapeutické plazmaferézové sezení. Použití diskrétní plazmaferézy v nepřítomnosti účinku léčby PN léky může zlepšit metabolické, hormonálně produkující funkce placenty a pomáhá normalizovat feto- a děložně-placentární průtok krve.
Léčba placentární nedostatečnosti je účinná, pokud první cyklus začíná před 26 týdny těhotenství a druhý po 32–34 týdnech. Léčba později zlepšuje stav plodu a zvyšuje odolnost vůči hypoxii, ale neumožňuje normalizovat jeho stav a zajistit odpovídající růst. Vysoký výskyt nepříznivých perinatálních výsledků během FGRM je do značné míry způsoben potřebou včasného porodu, pokud jde o
když se novorozenec dobře nepřizpůsobí vnějšímu prostředí (v průměru 31–33 týdnů). Při rozhodování o předčasném porodu zahrnuje komplex přípravy na porod kortikosteroidy pro prevenci komplikací v novorozeneckém období. Tyto léky nejen urychlují proces zrání plic plodu, ale také snižují četnost některých komplikací. Podle American National Institute of Health (1995) je výskyt intraventrikulárního krvácení a enterokolitidy u kojenců s SZRP nižší v pozorování prenatálních kortikosteroidů. Dexamethason je předepsán per os8-12-16 mg po dobu 3 dnů nebo IM 4 mg každých 12 hodin 4krát.
Je nutné vysvětlit ženě potřebu udržovat racionální stravu, spánek a odpočinek během těhotenství. Pacient by měl být vyškolen pro kontrolu tělesné hmotnosti, krevního tlaku. K diagnostice hypoxie by měla být žena trénována v počítání pohybů plodu po dobu 1 dne a vysvětlovat situace, ve kterých by měla okamžitě vyhledat lékařskou pomoc.
Kompenzovaný PN se vyznačuje příznivými perinatálními výsledky. K spontánnímu porodu přirozeným porodním kanálem dochází v 75,82% případů, bez komplikací - v 69,57%. Průběh narození s kompenzovaným PN je nejčastěji komplikován patologickým předběžným obdobím, progresí chronické nitroděložní hypoxie plodu, předčasným propuštěním plodové vody, slabostí a nekoordinací práce. Výskyt těchto komplikací těhotenství je indikací pro urgentní porodní operaci u 38,1% případů. Indikace pro plánovanou chirurgii císařského řezu jsou ve většině případů zatíženou porodnickou a gynekologickou anamnézou (včetně jizvy na děloze po předchozím císařském řezu, neplodnosti, syndromu ztráty těhotenství) v kombinaci s kompenzovaným PN, jakož i komplikovaným průběhem těhotenství, jakož i známkami poruchy plodu (FGRS I stupně, hemodynamické poruchy v systému matka-placenta-plod stupně IA nebo IB, počáteční známky hypoxie plodu), u žen starší věkové skupiny - v přítomnosti předjíždění těhotenství. Jak se závažnost PN zhoršuje, frekvence příznivého výsledku spontánní práce se snižuje, a proto
v případě subkompenzované PN je metodou volby plánované dodání císařským řezem v době blízké úplnému termínu.
Indikace pro plánovanou dodávku císařským řezem se subkompenzovanou ST jsou:
Středně těžká hypoxie plodu (snížení variability bazálního rytmu, počet zrychlení, jejich amplituda a trvání);
Hemodynamické poruchy v systému matka-placenta-plod II. Stupně v přítomnosti bilaterálních změn a dikrotických excizí v děložních tepnách;
S další porodnickou patologií;
Fetální růstový retardační syndrom v kombinaci s gestózou nebo prodlouženým těhotenstvím.
Kritéria pro prodloužení těhotenství se subkompenzovanou PN jsou:
Stupeň SZRP I-II v přítomnosti přiměřeného zvýšení fetometrických indikátorů v kontrolním ultrazvuku v intervalech 7 dnů;
SZRP III. Stupně bez zvýšení zpoždění fetometrických ukazatelů na pozadí neprogresivního porušování fetoplacentální cirkulace a / nebo počátečních příznaků centralizace krevního toku (LMS v fetální aortě více než 8,0 s hodnotami LMS v SMA 2,8-9,0 ve smyslu 33-37 týdnů);
Nepřítomnost výrazného porušení děložního průtoku krve (jednostranná, aniž by došlo k porušení spektra průtoku krve v děložních tepnách, SDO více než 2,4) s mírnou gestózou;
Nedostatek klinické progrese kombinované gestózy;
Počáteční příznaky hypoxie podle kardiotografie v nepřítomnosti nebo počáteční centralizaci arteriálního krevního oběhu v krvi, normální ukazatele orgánového (renálního) krevního toku plodu (SDO ne více než 5,2, pokud jde o 32 týdnů, a nejvýše 4,5, pokud jde o 33 až 37 týdnů);
Eukinetický a hyperkinetický typ centrální hemodynamiky plodu při absenci intrakardiální hemodynamiky.
Povoleno bylo komplexní studium fetální hemodynamiky a analýza perinatálních výsledků u placentární nedostatečnosti
vyvinout indikace pro urgentní doručení císařským řezem pro tuto patologii. Tyto zahrnují:
Kardiotocografické příznaky těžké fetální hypoxie (spontánní zpomalení na pozadí monotónního rytmu a nízké variability, pozdní zpomalení během testu oxytocinu);
Kritický stav průtoku krve plodu plodu s gestačním věkem více než 34 týdnů;
Těžké poruchy průtoku krve v žilním kanálu a spodní vena cava.
Indikace nouzového porodu je nástup porodu u těhotných žen se subkompenzovanou PN a také předčasné vypuštění plodové vody. Indikací pro přenos novorozence na jednotku intenzivní péče je prematurita, hypoxicko-ischemické poškození centrální nervové soustavy různé závažnosti.
Indikace pro urgentní doručení císařským řezem s dekompenzovaným PN:
Závažná MPS se známkami výrazné centralizace průtoku krve plodu s narušeným průtokem krve uvnitř srdce a příznaky mírné hypoxie plodu, podle CTG;
Progrese preeklampsie na pozadí komplexní terapie se závažným porušením uteroplacentálního krevního toku (bilaterální poruchy s dikrotickou excizí ve spektru);
Gestační věk v přítomnosti známek dekompenzované PN je více než 36 týdnů.
Indikace pro nouzové doručení:
Porušení žilního průtoku krve plodu (retrográdní průtok krve v žilním kanálu, zvýšení zpětného průtoku krve v dolní duté žíle), pulsace v pupeční šňůře;
Preeklampsie a eklampsie.
Při předčasném těhotenství (32–36 týdnů) a nepřítomnosti nulových a retrográdních hodnot průtoku krve v žilním kanálu během atriálního systolu a indexu pulzace až 0,74, s procentním podílem zpětného průtoku krve v dolní duté žíle až 43,2% až do 32 týdnů a až 34,1%, pokud jde o 32-37 týdnů, těhotenství by mělo být prodlouženo. Současně je prováděno komplexní ošetření s povinným intravenózním podáním roztoku instenonového pla
centrální nedostatečnost s denním dopplerometrickým a kardiotocografickým monitorováním. Komplex léčby zahrnuje glukokortikoidy pro urychlení zrání plodu.
Dodání se provádí císařským řezem, když se objeví známky progrese poruch žilního krevního toku nebo se objeví spontánní zpomalení, hypokinetický typ hemodynamiky a „dospělý“ typ fetálního krevního toku. Doba prodloužení těhotenství se pohybovala od 4 (v období 35-36 týdnů) do 16 dnů (v období 32-34 týdnů).
Včasná diagnóza placentární nedostatečnosti a SZRP, správná a kompetentní péče o těhotné ženy, vám umožní prodloužit těhotenství až do data narození životaschopného plodu s příznivým perinatálním výsledkem. Volba dodací lhůty by měla být založena na sadě diagnostických testů. Při včasném porodu je nutné vzít v úvahu podmínky pro intenzivní péči a resuscitaci novorozenců.
Děti s nízkou porodní hmotností mají později vysoké riziko zhoršení fyzického a psychického vývoje a zvýšené somatické morbidity. Nejčastěji v u novorozence jsou zaznamenány následující komplikace:
Poruchy kardiopulmonální adaptace s perinatální asfyxií, meconiální aspirace nebo perzistentní plicní hypertenze;
V kombinaci s SZRP s předčasně narozeným - vysoké riziko úmrtí novorozenců, nekrotické enterokolitidy, syndromu respirační tísně, intraventrikulárního krvácení;
Porušení termoregulace v důsledku zvýšení přenosu tepla (v důsledku poklesu v podkožní vrstvě) nebo snížení produkce tepla (vyčerpání katecholaminů a snížené dodávání živin);
Hypoglykémie (u 19,1% novorozenců);
Polycytémie a hyperkoagulabilita (diagnostikována u 9,5% u stupně I SZRP a u 41,5% u stupně III);
Snížená imunoreaktivita (u 50% novorozenců s III. Stupněm SZRP je detekována neutropenie, u 55% - nozokomiální infekce).
Děti s nízkou porodní hmotností mají různé možnosti fyzického vývoje v závislosti na etiologii a závažnosti
intrauterinní zpomalení růstu. Při mírné závažnosti respiračních potíží se během 6-12 měsíců po narození pozoruje vysoká míra růstu, během níž děti dosahují normálních vztahů mezi výškou a hmotností. Současně, podle některých zpráv, novorozenci dosáhnou normální tělesné hmotnosti do 6 měsíců po narození, ale zachovávají si růstový deficit 0,75 směrodatných odchylek během prvních 47 měsíců života ve srovnání s dětmi s normální tělesnou hmotností při narození. Při těžkých těžkých respiračních infekcích zůstávají děti v hmotnosti a výšce pod 10 %onejen v dětství, ale také v dospívání. Průměrná výška ve věku 17 let s těžkou retardací intrauterinního růstu je 169 cm u chlapců a 159 cm u dívek oproti 175 a 163 cm s normální tělesnou hmotností při narození.
Mnoho vědců s těžkým stupněm SZRP (porodní hmotnost méně než 3%), zejména u předčasných těhotenství, má snížení IQ a značné potíže s učením. Takže do věku 5 let, 2,4krát častěji než s normální tělesnou hmotností při narození, mají děti malé mozkové dysfunkce, motorické poruchy, dětskou mozkovou obrnu a špatné kognitivní schopnosti; 16% dětí ve věku 9 let potřebuje speciální vzdělání; 32% adolescentů s těžkým těžkým respiračním selháním má závažné problémy s učením, které jim brání v dokončení celého středního školního kurzu. Ve studii L.M. McCowan (2002), nízký index duševního vývoje (MDI), je nalezen u 44% novorozenců s SROP způsobenou těhotnou hypertenzí. Poruchy psychimotorického vývoje jsou nejčastěji zaznamenány u novorozenců, kteří kojili nejméně první 3 měsíce života, kteří byli v nemocnici po dlouhou dobu a vyžadují mechanickou ventilaci.
Placenta je dočasný orgán, který se tvoří pouze během těhotenství a plní funkci zásobování plodu vším potřebným pro zdravý vývoj. Placentární nedostatečnost se nazývá narušení její struktury a funkcí. Jiné sovy, jedná se o poruchu toku krve v systému plod-placenta-matka. V těžkých případech to může dokonce vést k úmrtí dítěte. Dozvíme se tedy o příčinách, terapii a důsledcích placentární nedostatečnosti.
Proč vznikla
Příčiny patologie jsou rozděleny na endogenní (působící zevnitř těla) a exogenní (působící z vnějšku). Jedná se o znečištění plynem, radiační expozici, stres, podvýživu, pracovní rizika, použití agresivních domácích chemikálií. Nadměrná fyzická námaha nastávající matky může také negativně ovlivnit stav placenty. Mezi exogenní faktory placentární nedostatečnosti patří špatné návykyZa prvé, kouření nastávající matky, pití alkoholu, vášeň pro silnou kávu.
Pokud jde o exogenní faktory, jedná se o věk budoucích žen pracujících nad 35 let a pod 18 let; četná narození a potraty; nádory vaječníků; historie hypotrofických dětí; obvyklý potrat; zánětlivé procesy genitálií.
Praxe ukazuje, že příčinou placentární nedostatečnosti jsou velmi často somatická onemocnění matky. Mluvíme o cukrovce, hypertenze, srdečních chorobách, nemocích krve a ledvin. Ohroženy jsou ženy s vrozenými patologiemi reprodukčních orgánů, například bicorn nebo sedlová děloha.
Léčba placentární nedostatečnosti
Hlavním cílem terapie je udržení těhotenství a včasného porodu.
Povinná hospitalizace žen s akutní formou placentární nedostatečnosti, retardace růstu plodu podle výsledků ultrazvuku a dopplerografie. Potřebují se plně uvolnit, racionálně jíst, trávit spoustu času na čerstvém vzduchu.
Aby se normalizoval průtok krve, jsou takovým pacientům předepisována léčiva, která zlepšují látkovou výměnu. Jsou to Actovegin, Troxevasin, kyselina askorbová, tokoferol. Ženy s takovou diagnózou jsou předepsány reocorrectors: Infucol, Reopoliglyukin, Reosorbilact. Je ukázáno zavedení síranu hořečnatého, eufillinu, glukózy a novokainu intravenózně.
Pro zlepšení vlastností krve jsou předepsány Trental a Curantil, Kleksan, Fraksiparin. Tyto léky ředí krev, brání výskytu patologických formací v placentě.
Budoucím matkám s narušenou funkcí placenty jsou předepsány léky, které zlepšují krevní oběh v mozku, například Piracetam, Nootropil. Obnovují výměnu plynu v placentě pomocí kyslíkové terapie navlhčeným kyslíkem a antihypoxanty. Tohle je Mildronate, Cytochrome C, Cavinton. Užívání sedativ je indikováno ke zmírnění podráždění mozku.
Léčba placentární nedostatečnosti zpravidla trvá při stacionárních podmínkách alespoň čtyři týdny. Poté, co se stav placenty zlepší, terapie pokračuje ambulantně. Obecná léčba trvá 6-8 týdnů. Jeho účinnost je hodnocena pomocí ultrazvuku, CT, Dopplerova ultrazvuku.
Dodání takových pacientů se přirozeně provádí pomocí zralého děložního čípku a kompenzované placentární nedostatečnosti. Doporučuje se porod s epidurální anestézií. Pokud dojde k oslabení práce, provede se stimulace prostaglandiny.
Brzy porod žen s placentární nedostatečností je indikován při absenci pozitivní dynamiky léčby a diagnostikované podvýživy plodu.
Důsledky patologie
Pokud těhotenství pokračuje na pozadí placentární nedostatečnosti, může se často rozvinout placentární narušení a předjíždění. Existuje riziko úmrtí plodu.
U dítěte hrozí taková diagnóza intranatální hypoxií se zhoršenou mozkovou cirkulací, neurologickými poruchami, sklonem k nachlazením, malformacemi.
Placentární nedostatečnost je syndrom způsobený morfologickými a funkčními změnami placenty, s progresí, ke které dochází k rozvoji PSA, která je často kombinována s hypoxií.
SYNONYMY PLACENTÁLNÍ NEDOSTATEČNOSTI
Fetoplacentální nedostatečnost je běžně používané synonymum, které nelze považovat za úspěšné, protože nemá správnou formu a podstatu.
KÓD MÍSTA NEZÁVADNOSTI PODLE ICD-10
Třída XV. Těhotenství, porod a šestinedělí (O00 - O99)
Péče o matku v souvislosti se stavem plodu, plodovou vodou a možnými potížemi při porodu (O30 - O48)
O36. Lékařská pomoc matce při jiných zjištěných nebo podezřelých patologických stavech plodu.
Třída XVI. Určité stavy vyskytující se v perinatálním období (P00 - P96)
Plod a novorozenec postižený mateřskými podmínkami, komplikace těhotenství, porodu a porodu (P00 - P04)
P02. Léze plodu a novorozence v důsledku komplikací placenty, pupeční šňůry a fetálních membrán. Poruchy související s délkou těhotenství a růstu plodu (P05 - P08)
P05. Zpomalený růst a podvýživa plodu.
P07 Poruchy spojené se zkráceným gestačním věkem a nízkou porodní hmotností jinde nezařazené.
EPIDEMIOLOGIE PLACENTÁLNÍHO NEDOSTATKU
Placentární nedostatečnost je jednou z nejčastějších těhotenských komplikací, vyskytuje se při potratu u 50–77%, s gestózou u 32%, s těhotenstvím a extragenitální patologií u 25–45%, u těhotných žen s virovou a bakteriální infekcí více než v 60% případů. PS u žen po placentární nedostatečnosti je 10,3% u novorozenců a 49% u předčasně narozených dětí. U 60% vede placentární nedostatečnost ke zpoždění vývoje plodu.
KLASIFIKACE PLACENTÁLNÍ POJIŠTĚNÍ
Byla vyvinuta široká škála klasifikací placentární nedostatečnosti. Některé z nich jsou podmíněné. Nejběžnější a akceptované jsou následující klasifikace.
Druhy placentární nedostatečnosti v čase a mechanismus výskytu.
· Primární - vyskytuje se až 16 týdnů těhotenství a je spojena s narušenými procesy implantace a placentace.
· Sekundární - vyvíjí se na pozadí již vytvořené placenty (po 16. týdnu těhotenství) pod vlivem faktorů exogenních pro plod a placentu.
Druhy placentární nedostatečnosti v klinickém průběhu:
· Akutní - nejčastěji spojené s oddělením normální nebo nízko umístěné placenty, vyskytuje se hlavně při porodu.
· Chronická - může se vyskytnout v různých stádiích těhotenství.
- Kompenzované - metabolické procesy v placentě jsou narušeny, nedochází k porušení uteroplacentální a fetoplacentální cirkulace (podle Dopplerových studií v tepnách funkčního systému matka-placenta-plod).
- Decompensated - stanoví se porušení uteroplacentální a / nebo placentární cirkulace (podle Dopplerometrických studií v tepnách funkčního systému matka-placenta-plod).
Rozlišují se následující stupně geodynamických poruch v tepnách funkčního systému matka-placenta-plod.
· Stupeň I - narušení děložního nebo fetoplacentálního krevního toku.
· Stupeň II - narušení toku krve z dělohy a placenty.
· Stupeň III - centralizace fetoplacentálního krevního toku, zhoršený tok krve dělohy.
· Stupeň IV - kritická porušení fetoplacentálního průtoku krve (nulový nebo reverzní diastolický průtok krve v pupeční tepně nebo aortě, zhoršený tok krve dělohy).
Druhy placentární nedostatečnosti přítomností retardace růstu plodu (PSA).
· Placentární nedostatečnost bez PSA.
· Placentární nedostatečnost s PSA.
ETIOLOGIE (DŮVODY) PLACENTÁLNÍ NEDOSTATEČNOSTI
Placentární nedostatečnost je připisována polyetiologickým onemocněním.
Příčiny placentární nedostatečnosti.
Mezi nimi jsou podmíněně rozlišovány endo a exogenní.
· Endogenní příčiny. Způsobují různé možnosti narušení placentace a zrání klků, ve kterých se může vyvinout vaskulární a enzymatická nedostatečnost, což vede k tvorbě primární placentární nedostatečnosti.
· Exogenní příčiny. Zahrnují významný počet různých faktorů, jejichž působení vede k narušení oběhu uteroplacentální a fetoplacentální. V důsledku jejich vlivu se nejčastěji tvoří sekundární placentární nedostatečnost.
Příčiny primární placentární nedostatečnosti:
Genetické faktory
· Bakteriální a virové infekce;
· Endokrinní faktory (hormonální selhání vaječníků atd.);
· Enzymatický deficit deciduální tkáně, která působí jako živná půda pro vyvíjející se vajíčko plodu.
Tyto faktory vedou k anatomickým poruchám ve struktuře, umístění, připojení placenty, stejně jako defektům v angiogenezi a vaskularizaci, zhoršené diferenciaci choriových klků. Soubor patologických procesů zodpovědných za rozvoj primární placentární nedostatečnosti je často pozorován během potratu, zejména při obvyklém těhotenství a těhotenství, ke kterému dochází po neplodnosti.
Příčiny sekundární placentární nedostatečnosti. Vyvíjí se s porodními chorobami a těhotenskými komplikacemi.
Nedávné studie prokázaly konvenčnost rozdělení placentární nedostatečnosti na primární a sekundární. Primární placentární nedostatečnost se ve velkém procentu případů může proměnit v sekundární a sekundární placentární nedostatečnost se často tvoří na pozadí subklinických patologických procesů v časných stádiích těhotenství. Latentní porušení placentace může způsobit časný výskyt klinických projevů placentární nedostatečnosti a její závažný průběh v druhé polovině těhotenství. K tomu dochází, když těhotná žena má porodnická onemocnění a těhotenské komplikace, jako je gestóza, hrozící ukončení těhotenství, vícenásobné těhotenství; extragenitální onemocnění (hypertenze, onemocnění srdce a ledvin, diabetes).
Kvůli rozmanitosti, různorodosti a nejednoznačnosti působení etiologických faktorů, které mohou způsobit rozvoj placentární nedostatečnosti, existují rizikové faktory pro vývoj placentární nedostatečnosti: sociální, porodnická a extragenitální onemocnění, vrozená a dědičná patologie u matky a plodu a vnější faktory.
Rizikové faktory pro placentární nedostatečnost:
· Sociální faktory: věk matky nad 30 let a mladší 18 let, podvýživa, těžká fyzická práce, psychoemocionální přetížení, nebezpečí z povolání, kouření, požívání alkoholu a drog;
· Mimoděložní onemocnění: onemocnění kardiovaskulárního systému, ledviny, plíce, onemocnění krevního systému, cukrovka;
· Porodnické a gynekologické faktory:
- anamnestické (menstruační dysfunkce, neplodnost, potrat, narození předčasně narozených dětí);
- gynekologické (abnormality reprodukčního systému, děložní myomy);
- porodnické a mimoděložní nemoci během skutečného těhotenství (gestóza, hrozící potrat, vícenásobné těhotenství, abnormality v umístění a připojení placenty, infekce, včetně urogenitální, APS, aloimunní cytopenie);
· Vrozená a dědičná patologie u matky nebo plodu;
· Vnější faktory: ionizující záření, fyzikální a chemické účinky, včetně drog.
Mezi nejvýznamnější rizikové faktory pro vývoj placentární nedostatečnosti patří gestóza a kombinace těhotenství s extragenitální patologií, doprovázené cévním poškozením. Různé etiologické faktory působící v různých stádiích vývoje a fungování placenty jsou nakonec zapojeny do obecného patogenetického mechanismu vedoucího k rozvoji syndromu placentární nedostatečnosti, přičemž jeden z hlavních projevů je považován za porušení placentární cirkulace - hlavní funkce placenty.
PATHOGENESA PLACENTÁLNÍHO NEDOSTATKU
Hlavní roli v patogenezi placentární nedostatečnosti hraje narušení uteroplacentální perfuze, což vede ke snížení transportu kyslíku a živin přes placentu do plodu. Výskyt hemodynamických poruch v placentě je spojen s porušením morfologických a biochemických adaptačních reakcí v placentě během fyziologického těhotenství. Protože vývoj struktur a funkcí placenty nastává ve stádiích, patologické změny, které se vyskytují v placentě, závisí na povaze a době expozice nepříznivým faktorům.
Fáze narušení uteroplacentální cirkulace: narušení migrace endovaskulárních trofoblastů, nedostatečnost invaze extravillousového chorionu, narušená diferenciace placentárních klků.
· Porušení endovaskulární migrace trofoblastů v prvním trimestru těhotenství vede ke zpoždění tvorby uteroplacentální cirkulace s tvorbou nekrotických změn v placentárním loži až do jeho úplného vymezení a následné smrti embrya.
· Nedostatečná invaze extravilárního choria vede k neúplné transformaci spirálních tepen, což je považováno za jeden z hlavních mechanismů pro snížení uteroplacentálního oběhu s rozvojem placentární hypoplasie a fetální hypotrofie. V důsledku toho se část spirálních tepen netransformuje po celé své délce, v druhé části se transformace vyskytují pouze v jejich decidual segmentech, aniž by byly ovlivněny myometrické, což zachovává schopnost krevních cév reagovat na vazokonstrikční stimuly.
· Poruchy diferenciace placentárních klků mají velký význam v patogenezi placentární nedostatečnosti. Projevují se jejich opožděným vývojem, předčasným stárnutím nebo nerovnoměrným zráním s přítomností klků všech typů v placentě. V tomto případě jsou procesy tvorby syncytiokapilárních membrán narušeny a / nebo placentární bariéra zesiluje v důsledku akumulace kolagenu a procesů fibroblastů v bazální vrstvě, proti které jsou bráněny metabolické procesy přes placentární membránu.
Faktory přispívající k narušení uteroplacentární perfuze: porodnická a mimoděložní onemocnění matky, u kterých dochází ke snížení průtoku krve do intervillousního prostoru (preeklampsie, hypertenze atd.), Zpomalení krevního toku v něm na pozadí obtíží při odtoku krve a lymfy (preeklampsie a kardio) cévní onemocnění s edematózním syndromem, hrozba ukončení těhotenství s prodlouženým zvýšeným tónem dělohy), zvýšená viskozita krve.
Důsledky porušení uteroplacentálního oběhu. Porušení uteroplacentálního krevního toku vede k ischémii, narušené mikrocirkulaci, ukládání imunitních komplexů v trofoblastu, narušené struktuře, nerovnováze mezi větvením a nerozvětvením angiogeneze, narušenému transportu kyslíku a živin placentou a dodávce kyslíku do plodu.
Ischémie Snížení objemové rychlosti průtoku krve v intervillousním prostoru vede k ischemii, za níž podmínky aktivace lipidové peroxidační soustavy s tvorbou volných kyslíkových radikálů, uvolňování elastázy z aktivních neutrofilů, což způsobuje poškození vaskulárního endotelu. V endotelu dochází ke snížení syntézy cytoprotektorů a vazodilatátorů: prostacyklinu a endoteliálního relaxačního faktoru (oxid dusnatý).
· Porušení mikrocirkulace. Uvolnění zvýšeného množství tkáňového tromboplastinu, zvýšení agregace a adheze destiček, zvyšuje syntézu tromboxanu A2 a endotelinu, který má vazokonstrikční účinek. Dochází k patologickému zvýšení indexu tromboxan / prostacyklin. V oblastech endoteliálního poškození se ukládají fibriny, lipidové depozity, zvyšuje se počet receptorů, které vážou vazopresorové látky, což vede ke zvýšenému vaskulárnímu odporu, proti kterému se snižuje průtok krve děložním placentem.
· Depozice imunitních komplexů v trofoblastu. S dalším narušením mikrocirkulačních procesů v tkáních placenty stimulují buňky poškozeného endotelu, které hrají roli Ar, produkci protilátek s ukládáním imunokomplexů pod endothelium trofoblastových cév.
Porušení struktury syncytiotrofoblastu. V budoucnu se vlivem cytotoxických látek průtok krve v intervillousním prostoru ještě více zpomalí, což přispívá k výraznějšímu poškození endotelu. Vytváří se tak „začarovaný kruh“ hemodynamických poruch v placentě.
Nerovnováha mezi větvením a nerozvětvením angiogeneze. Ve stadiu vývoje villusového stromu může střední hypoxie stimulovat proliferativní schopnost cytotrofoblastu, transkripci vaskulárního endoteliálního faktoru, angiogenezi větvového typu s rozvojem nadměrné kapilizace klků.
Současně se zvyšuje hmotnost placenty, díky čemuž je kompenzována nedostatečná uteroplacentární perfuze a po dlouhou dobu je zachována normální vaskulární rezistence v placentární tkáni. Ve většině případů je však pod vlivem hypoxie stimulován placentární růstový faktor, což vede ke snížení angiogeneze větvícího typu, která nahrazuje nerozvětvenou angiogenezi, s tvorbou výrazného nedostatku kapilár klků. V důsledku toho neexistuje rovnováha mezi větvením a nerozvětvenou angiogenezí, která ve druhé polovině těhotenství podporuje normální vývoj cévní sítě placenty.
Porušení placentární angiogeneze a absence tvorby normálního vilusového stromu vede k oběhovým poruchám (vyskytují se brzy), což vede k časnému rozvoji PSA. Nedostatek výměnné plochy placenty je způsoben hlavně snížením počtu arteriol terciálních klků, a to jak z důvodu jejich nedostatečné tvorby, tak zničení v důsledku tromboembolických a vazospastických procesů.
Placenta se vyznačuje vysokou mírou metabolismu a spotřebovává více než polovinu veškerého kyslíku a více než čtvrtinu celkového množství glukózy pocházející z krevního toku matky, a proto je při nedostatečném uteroplacentárním oběhu primárně poškozena.
Porušení transportu kyslíku a živin placentou. Transport kyslíku a látek placentou se provádí dvěma hlavními mechanismy: difúzí a aktivním transportem.
Schopnost placenty transportovat se zvyšuje s rostoucím gestačním věkem, což je způsobeno procesy zrání a diferenciace trofoblastu. Transportní funkce závisí na intenzitě uteroplacentálního a placentárního toku, propustnosti placentární bariéry, stavu aktivních transportních systémů, úrovni metabolismu placenty, metabolismu u matky a plodu.
Poruchy šíření. Dodávání kyslíku a oxidu uhličitého do plodu nastává jednoduchou nebo usnadněnou difúzí a závisí na intenzitě průtoku krve v intervilním prostoru. Snížená oxygenace placentárních tkání vede k nedostatku energie a v důsledku toho k narušení aktivních transportních systémů.
Porušení aktivní dopravy. Aktivním transportem se přes placentární bariéru přenášejí aminokyseliny, proteiny, peptidové hormony, vitamíny a další látky.
Výsledkem je změna aktivity syntetických procesů v placentě, která se v prvních stádiích vyznačuje kompenzační hyperprodukcí většiny enzymů, po které je nahrazena jejich vyčerpáním. Ve většině případů vede primární narušení uteroplacentární perfúze a ischémie v tkáních placenty k druhému narušení transportní funkce a buněčné-parenchymální nedostatečnosti, která je charakterizována změnou aktivity enzymů a stavu buněčného metabolismu. V některých situacích, například při narušení diferenciace klků, však může syntetická funkce placenty trpět především.
Porucha dodávky kyslíku do plodu. V závislosti na závažnosti poklesu dodávek kyslíku do plodu se rozlišují tři po sobě jdoucí fáze tohoto chronického patologického procesu: hypoxémie, hypoxie a asfyxie.
Hypoxémie je charakterizována snížením obsahu kyslíku v arteriální krvi plodu. V jeho těle se adaptivní reakce vyvíjejí postupně.
- Stimulace krvetvorby, včetně extramedulární, v jejímž důsledku se vyvíjí polycytémie, která se vyznačuje zvýšením počtu cirkulujících červených krvinek a zvýšením hladiny hematokritu.
- V počátečních stádiích je aktivována glukoneogeneze v játrech, je však snížena schopnost akumulovat glukózu ve formě glykogenu. Transport glukózy do plodu je omezený, což za podmínek nedostatku energie vede k postupnému narušení mechanismů aktivního transportu v placentě.
- Při zvýšení hypoxémie se srdeční výdej přerozděluje: životně důležité orgány (mozek, srdce, nadledvinky) jsou zásobovány hlavně krví.
- Snížení rychlosti růstu plodu až do úplného zastavení. Významnou roli v těchto procesech hraje nedostatek inzulínu v krvi plodu, který je zodpovědný za přenos glukózy placentou a její využití v kosterním svalu, játrech a tukové tkáni.
Hypoxie. V důsledku nedostatečného obsahu intracelulárního kyslíku nezbytného pro aerobní metabolismus a vytvoření dostatečné energie se vyvíjí „hypoxický stres“, doprovázený uvolňováním biologicky aktivních látek a hormonů, včetně adrenalinu a norepinefrinu. To vede k ještě výraznějšímu redistribuci krevního toku směrem k životně důležitým orgánům: aktivují se aortální baro- a chemoreceptory, vazokonstrikce břišní aorty, mezenterické tepny acévy kosterních svalů. V důsledku nárůstu hypoxie, hypoglykémie a nedostatku energie přechází metabolismus glukózy na anaerobní cestu, která není schopna kompenzovat nedostatek energie. Anaerobní produkty glykolýzy přispívají k rozvoji metabolické acidózy.
Asfyxie. Další zvýšení závažnosti patologického procesu vede k rozvoji stavu kritického pro přežití plodu. Možná ztráta mechanismů, které zajišťují centralizaci toku krve plodu, v důsledku čehož je narušena dodávka krve do životně důležitých orgánů. V tomto případě odpovídá povaha průtoku krve v periferních cévách toku krve v pupeční tepně - nedochází k translačnímu pohybu krve do diastolické fáze nebo dochází k retrográdnímu průtoku krve. Za těchto podmínek je možné udržovat energetickou rovnováhu životně důležitých orgánů pouze po krátkou dobu, po které se buňky a tkáně těchto orgánů přepnou na anaerobní cestu metabolismu. Tento proces charakterizuje začátek závěrečné fáze nedostatku kyslíku - asfyxie, proti níž dochází v buňkách vitálních orgánů k nevratným změnám a dochází k konečné dekompenzaci, která vede k úmrtí plodu. PN, doprovázený vážnými metabolickými a hemodynamickými poruchami ve funkčním systému matky-placenty, vede k rozvoji PSA - jedné z hlavních příčin perinatální morbidity a PS.
KLINICKÉ OBRÁZEK \u200b\u200b(SYMPTOMY) PLACENTÁLNÍ NEDOSTATEČNOSTI
U chronických PN představují těhotné ženy stížnosti charakteristické pro porodnická a extragenitální onemocnění, proti nimž se vyvíjí chronická nebo akutní PN. Lze však zaznamenat pokles počtu fetálních pohybů. U akutního PN během porodu mohou být pozorovány klinické příznaky ENDL.
DIAGNÓZA PLACENTÁLNÍHO NEDOSTATKU
ANAMNÉZA
Při sběru anamnézy jsou objasněna anamnestická data, která lze přiřadit PN mateřským, fetálním nebo placentálním rizikovým faktorům pro vývoj PN (viz oddíl „Etiologie“). Zvláštní pozornost by měla být věnována přítomnosti klinických příznaků ohroženého potratu, gestózy.
FYZICKÁ STUDIE PRO PLACENTÁLNÍ POJIŠTĚNÍ
Těhotné rizikové skupiny pro vývoj PN vyžadují pravidelné klinické pozorování. Při porodním vyšetření byste měli věnovat pozornost těmto znakům:
· Výška a hmotnost těhotné ženy;
· Obvod břicha, VDM (je-li rozdíl v numerické hodnotě gestačního věku a VDM, vyjádřený v centimetrech, větší než tři, můžeme mluvit o přítomnosti PSA; toto kritérium umožňuje identifikovat asi 50% těhotenství komplikovaných PSA);
Děložní tón (zvýšený s hrozbou ukončení těhotenství);
· Dostupnost špinění z genitálního traktu;
· Počet pohybů plodu, povaha srdečního rytmu během auskultace (hluchota srdečních zvuků a změna srdeční frekvence).
LABORATORNÍ VÝZKUM V MÍSTĚ NEZÁVADNOSTI
Mají diagnostickou hodnotu pro identifikaci rizikových skupin u pacientů, které nemají podvýživu plodu, kompenzované PN v trimestru III těhotenství. Laboratorní studie jsou zaměřeny na hodnocení hormonální funkce placenty:
· Stanovení celkové a placentární alkalické fosfatázy v krevním séru s následným stanovením jejího podílu na celkové aktivitě fosfatázy;
· Stanovení sérových hladin PL a oxytocinázy;
· Vylučování moči močí.
Kromě výše uvedených studií je laboratorní diagnostika prováděna v souladu s algoritmem pro zkoumání porodnických a mimoděložních chorob, proti nimž se vyvinul PN syndrom.
NÁSTROJOVÝ VÝZKUM V MÍSTNĚ NEZÁVADNOSTI
Nejčastěji se mezi instrumentální metody pro diagnostiku ST používají ultrazvuk a CTG. Ultrazvukové metody hrají hlavní roli v diagnostice PN a PSA. V trimestru těhotenství II a III provádí ultrazvukové vyšetření (20–24 týdnů a 30–34 týdnů), jakož i další indikace, ultrazvukovou fetometrii a Dopplerometrické vyšetření průtoku krve v tepnách a žilách funkčního systému matka-placenta-fetal.
Při provádění ultrazvuku kromě fetometrie, která vám umožňuje stanovit diagnózu PSA, byste měli věnovat pozornost následujícím charakteristikám:
· Určení umístění placenty, její tloušťky a struktury (stupeň zralosti, přítomnost otoků, rozšíření intervilních prostor atd.);
· Identifikace nízké nebo vysoké vody (měření největší vertikální kapsy nebo výpočet indexu AF);
· Identifikace ultrazvukových příznaků těch porodnických a mimoděložních nemocí, které jsou základem rozvoje placentární nedostatečnosti;
· Výzkum a hodnocení v bodech biofyzikálního profilu plodu (pokud je vybaven). Tzv. Reaktivita srdeční frekvence plodu se hodnotí podle CTG (přítomnost motoricko-srdečního reflexu), respiračního rytmu, obecné motorické aktivity, tónu a objemu OM. Při normálním funkčním stavu plodu je celkové skóre jeho biofyzikálního profilu 10 bodů.
Dopplerometrické studium toku krve v tepnách a žilách funkčního systému matka-placenta-plod je považováno za hlavní diagnostickou metodu, jejíž výsledky charakterizují stav placentárního oběhu a jeho soulad s potřebami plodu během trimestru II a III těhotenství. Absence narušení uteroplacentální a fetoplacentální cirkulace naznačuje normální fungování placenty.
· Studie průtoku krve v tepnách. Nejčastěji je vyšetřován průtok krve v děložních tepnách, pupečních tepnách a střední mozkové tepně plodu.
Vyšetřovaná plavidla.
- děložní tepny. U poruch oběhu je charakteristický pokles diastolické složky na křivce rychlosti proudění krve. Tvorba patologických křivek rychlosti průtoku krve v děložních tepnách je založena na neúplné invazi trofoblastu do spirálních tepen, což vede ke zvýšení rezistence ve fondu děložních tepen.
- tepna pupeční šňůry. Patologické křivky rychlosti průtoku krve v pupeční tepně, jejímž jediným periferním kanálem je vaskulatura fetální části placenty, jsou poklesem diastolické složky v křivce rychlosti toku krve, stejně jako v děložní tepně. Zvýšení vaskulární rezistence placenty je způsobeno poškozením mikrovláken klků.
- Střední mozková tepna plodu. Nejstudovanější mozkovou cévou plodu je střední mozková tepna. Jeho křivka rychlosti proudění krve má tvar charakteristický pro vaskulární systém s vysokým odporem. Patologické křivky ve střední mozkové tepně (na rozdíl od křivek v pupeční šňůře a děložních tepnách) se vyznačují zvýšením rychlosti diastolického průtoku krve (tzv. Centralizace).
Indikátory pro hodnocení povahy křivky rychlosti proudění krve. Pro posouzení povahy křivky rychlosti průtoku krve se vypočítá jeden z následujících indikátorů vaskulární rezistence.
- systolicko-diastolický přístup.
- Index odporu.
- Index zvlnění.
Patologické hodnoty jsou považovány za hodnoty, které pro těhotenský věk přesahují 90%.
- Cerebro-placentární poměr - hodnota poměru IR ve střední mozkové tepně k IR ve pupeční tepně, která ve fyziologických podmínkách přesahuje 1,0. Snížení tohoto ukazatele o méně než 1,0 znamená přerozdělení toku krve plodu směrem k životně důležitým orgánům, především mozku (fenomén centralizace fetoplacentální cirkulace).
Přítomnost změn hemodynamických parametrů během dopplerografie není totožná s hypoxií. S vysokou pravděpodobností můžeme hovořit o hypoxii při registraci tzv. Kritických ukazatelů fetoplacentální cirkulace (s nulovým a reverzním diastolickým průtokem krve v pupeční tepně, předporodní úmrtnost je asi 50%).
· Studie průtoku krve v žilách. Pokud jsou zaznamenány kritické hodnoty průtoku krve v tepnách fetální-placentární cirkulace, je v tomto systému vyšetřena žilní cirkulace. Jsou prováděny dopplerografické studie pupečníkové žíly, venózního kanálu, dolní duté žíly a jugulárních žil plodu.
Nepříznivé známky poškození žilní cirkulace (patologické křivky rychlosti proudění krve)
- Žíla pupeční šňůry. Zachování pulsace po 16. týdnu těhotenství. Známka označuje kardiovaskulární dekompenzaci plodu.
- Žilní potrubí. Absence orthograde krevního toku ve všech fázích srdečního cyklu, což naznačuje porušení
okysličování životně důležitých orgánů.
- Nižší vena cava. Porušení odtoku krve z dolní poloviny těla plodu.
- Krční žíly plodu. Porušení odtoku krve z horní poloviny těla plodu.
Kardiotocografie
Diagnostická kritéria pro těhotenství byla vyvinuta po dobu 32 týdnů nebo déle (viz kapitola „Instrumentální neinvazivní metody výzkumu“).
· Nejvýznamnější diagnostická kritéria pro zhoršený funkční stav plodu během těhotenství:
Snížená amplituda motorického srdečního (myokardiálního) reflexu a / nebo
- snížení amplitudy kmitů srdečního rytmu.
Je třeba si uvědomit, že pokles amplitudy lze pozorovat nejen v případě narušení funkčního stavu plodu, ale také v souvislosti se zaznamenáváním v období klidového stavu plodu v cyklu odpočinku aktivity, patologické nezralosti centrálního nervového systému plodu proti placentární nedostatečnosti a užíváním léků těhotné ženy.
· Hlavním diagnostickým znakem narušení funkčního stavu plodu během porodu je povaha reakce srdečního rytmu plodu na kontrakce
· Studium cyklické organizace funkčních stavů (vytvoření cyklu „aktivita-odpočinek“). Za fyziologických podmínek se aktivita - cyklus odpočinku tvoří do 34–35 týdnů těhotenství. Zpoždění nebo nedostatek tvorby cyklu naznačuje narušení funkčního stavu centrálního nervového systému plodu (opožděné zrání jeho koordinační a integrační funkce) na pozadí placentární nedostatečnosti.
PROMÍTÁNÍ
Ultrazvuková diagnostika během těhotenství musí být provedena třikrát v období 11-14, 20-24 a 32-34 týdnů.
ÚDAJE O KONZULTACI OSTATNÍCH ZNALCŮ
Potřeba konzultace závisí na porodnické a mimogenetické patologii, na jejímž pozadí se rozvíjí placentární nedostatečnost.
PŘÍKLAD FORMULACE DIAGNÓZY PRO PLACENTÁLNÍ POJIŠTĚNÍ
PONRP. Akutní nedostatečnost placenty. Hypoxie plodu.
Chronická kompenzovaná placentární nedostatečnost.
Chronická kompenzovaná placentární nedostatečnost. ZRP.
Chronická dekompenzovaná placentární nedostatečnost. I stupeň hemodynamických poruch.
Chronická dekompenzovaná placentární nedostatečnost. Kritické fetoplacentální poruchy
průtok krve. ZRP.
ZPRACOVÁNÍ MÍSTNOSTI NEZÁVADNOSTI
CÍLE OŠETŘENÍ
Vývoj placentární insuficience je spojen s morfologickými změnami placenty, na jejímž pozadí vznikají především hemodynamické poruchy, a proto není možné dosáhnout vyléčení těchto procesů. Hlavním cílem léčby je prodloužení těhotenství a včasného porodu.
· Prodloužení těhotenství se provádí optimalizací krevního oběhu a opravou metabolických poruch v placentě v přítomnosti významné nezralosti plodu (až do 34 týdnů těhotenství) a neschopnosti poskytnout mu po porodu dostatečnou novorozeneckou péči.
· Včasný výběr termínu a způsobu porodu, kdy plod dosáhne životaschopného období pro existenci mimomateriálů (obvykle po 34 týdnech těhotenství). To vyžaduje přiměřenou diagnózu stupně narušení funkce placenty.
ÚDAJE O HOSPITALIZACI V MÍSTNÍ NEZÁVADNOSTI
Indikace pro hospitalizaci v porodnické nemocnici jsou stanoveny individuálně s přihlédnutím k souběžné patologii.
Indikace během těhotenství a před porodem.
Indikace během těhotenství:
- dekompenzace (podle Dopplerometrie) cirkulace placenty, bez ohledu na její stupeň;
- porušení funkčního stavu plodu zjištěného jinými diagnostickými metodami;
- přítomnost systémů protivzdušné obrany.
LÉČIVÉ LÉČENÍ PLACENTÁLNÍ POJIŠTĚNÍ
Terapie placentární nedostatečnosti je do značné míry určována potřebou řešit příčiny poruch oběhu v placentě. U pacientů s hrozbou přerušení je důležitou součástí léčby placentární insuficience snížení tónu děložních svalů; s gestózou - eliminace angiospasmu a zlepšení mikro a makrohemodynamiky. Je také důležité provádět patogeneticky podloženou terapii u onemocnění, jako je hypertenze, diabetes, APS atd.
Komplexní patogenetická terapie placentární nedostatečnosti
Komplexní patogenetická terapie placentární nedostatečnosti zahrnuje především léky s vazoaktivním účinkem. Pro zlepšení oběhu placenty je vhodné použít kombinaci Actoveginu s b-adrenergními agonisty. Actovegin © je předepsán jako intravenózní infuze: 80–160 mg (2–4 ml) Actoveginu © ve 200 ml 5% roztoku glukózy. Počet infuzí závisí na dynamice dopplerometrických ukazatelů ve fetoplacentální cirkulaci (až 10 infuzí). V budoucnu je možné použít Actovegin © a hexoprenalin perorálně: Actovegin © ve formě tablety s prodlouženým účinkem (200 mg), 1 tableta denně, 0,5 mg hexoprenalinu 1 / 4–1 / 2 tablety dvakrát až šestkrát denně.
V posledních letech rozšířené používání v porodnické praxi k prevenci nemocí, které způsobují rozvoj placentární nedostatečnosti a její léčby, používají protidestičková činidla: dipyridamol, pentoxifylin. Na protidestičkové látky používané v porodnictví se vztahují tyto požadavky:
· Nedostatek teratogenních a embryotoxických účinků;
· Normalizace poměru GHG zvýšením syntézy GHG P-I2;
· Zlepšení mikrocirkulace a průtoku placenty krví;
· Nedostatek rizika krvácení a oslabení hypotenzivního účinku léků používaných k léčbě gestózy.
Indikace pro užívání protidestičkových látek:
· Onemocnění kardiovaskulárního systému (srdeční vady, hypertenze, křečové žíly dolních končetin);
· Chronická onemocnění ledvin a jater;
Tromboflebitida a žilní trombóza;
· Endokrinní choroby (diabetes atd.);
· AFS;
· DIC
Nejbezpečnějším protidoštičkovým činidlem a angioprotektorem je dipyridamol. Může být použit kdykoli během těhotenství a v kombinaci s antihypertenzivy, kyselinou acetylsalicylovou, heparinem. Zlepšuje mikrocirkulaci v placentě zvýšením intenzity kolaterálního krevního toku, zvýšením syntézy P-I2, snížením aktivace a agregací destiček. Lék jako prostředek prevence a léčby placentární nedostatečnosti u těhotných žen s gestózou je předepisován v dávkách 75-225 mg / den. Jeho maximální denní dávka je 450 mg. Při užívání dipyridamolu neexistuje nebezpečí předávkování a rozvoje krvácení, takže léčivo může být použito až do porodu, a je-li to nutné, počínaje prvními dny po narození.
Pokud je těhotenství kombinováno se závažnými formami inzulín-dependentního diabetu, stejně jako u žen, které mají AFS jako příčinu nežádoucích těhotenských výsledků, hepariny s nízkou molekulovou hmotností a heparinoidy (fraxiparin, sulodexid) jsou účinné v prevenci a léčbě placentární nedostatečnosti. Načasování a trvání léčby těmito léky by se v každém případě mělo zvolit individuálně. Kromě toho se u APS jako hlavní prostředek používají intravenózní imunoglobuliny, kromě protidestičkových látek a heparinů s nízkou molekulovou hmotností a rybí tuk a wobenzym © se doporučuje jako další terapie.
V poslední době byla upřednostňována léčiva kombinovaného vazoaktivního a metabolického typu.
Například pro hemodynamická poškození v systému matka-placenta-fetální iv se přikape 5,0 ml 10% roztoku trimethylhydrazinium propionátu ve 200 ml 0,9% PPA NaCl nebo 5% roztoku glukózy, s výhodou v kombinaci se zavedením 5,0 ml 5% kyseliny askorbové. Lék má neuroprotektivní účinek, nemá účinek „okrádání“; jeho působení je reverzibilní.
PODMÍNKY A METODY DODÁVÁNÍ
Hlavní příčinou akutní a chronické hypoxie plodu, jakož i narození dětí s neurologickými poruchami, je placentární nedostatečnost, takže výběr optimálního načasování a způsobu porodu žen s touto patologií může výrazně snížit perinatální ztráty.
Při identifikaci příznaků funkční poruchy plodu podle klinických, laboratorních a instrumentálních údajů před nástupem porodu se rozhoduje o otázce načasování a způsobu porodu individuálně, přičemž se vezme v úvahu především závažnost identifikovaných poruch, připravenost porodního kanálu pro porod a celková porodnická a mimoděložní onemocnění těhotné ženy.
Indikace pro předčasné ukončení těhotenství (s gestačním věkem nad 30–32 týdnů):
· Kritické zhoršení fetoplacentálního průtoku krve;
· III. Stupeň poruch funkčního systému matky-placenty.
Perinatální výsledky při dřívějším porodu jsou pochybné. Způsob volby pro dodání v zájmu plodu je císařský řez. Při identifikaci symetrické formy PSC by měla být nejprve odstraněna chyba při stanovení gestačního období a poté by měla být vyloučena přítomnost chromozomální patologie u plodu. V případě placentární nedostatečnosti s hemodynamickými poruchami stupně I - II není vhodné prodloužit těhotenství o 37 týdnů.
Indikace pro předčasné ukončení těhotenství s neúčinností prodlouženého těhotenství (do 37. týdne těhotenství):
· Absence pozitivní dynamiky u indikátorů fetometrie a / nebo dopplerometrie po 10denní léčbě placentární nedostatečnosti;
Podvýživa plodu.
Při absenci biologické připravenosti měkkého porodního kanálu pro porod, přítomnost VZRP se známkami zhoršeného funkčního stavu plodu u primiparous starších dětí s zatíženou porodnickou a gynekologickou historií, je výběrem metody porodu císařský řez.
Indikace pro řízení práce přirozeným porodním kanálem: příznivá porodnická situace a uspokojivé ukazatele plodu (podle ultrazvuku, CT, Doppler, funkční zátěžové testy).
V tomto případě by se hlavní pozornost měla věnovat včasné přípravě porodního kanálu (řasy, dinoprostonu), monitorovat monitorování plodu, přiměřené úlevu od bolesti.
Pokud je porod plánován prostřednictvím porodního kanálu, je práce prováděna s časnou amniotomií za neustálého sledování funkčního stavu plodu pomocí přímého CTG. Pokud je to nutné, je vhodné provést Zalingův test během porodu.
VYHODNOCENÍ ÚČINNOSTI LÉČEBNÉ NEDOSTATEČNOSTI
· Fetometrické ukazatele se určují jednou za dva týdny.
· Frekvence dopplerovského studia cév funkčního systému matka - placenta - plod závisí na stupni hemodynamických poruch.
· Dynamické monitorování funkčního stavu plodu pomocí CTG se provádí nejméně jednou týdně.
PREVENCE PLACENTÁLNÍ POŽADAVKY
Zahrnuje širokou škálu protidrogových a protidrogových opatření.
· Léčba porodnických a extragenitálních chorob predispozice k rozvoji placentární nedostatečnosti.
· Regulace tkáňového metabolismu a redoxních procesů u těhotných rizikových skupin pro vývoj placentární nedostatečnosti. Za tímto účelem se předepisují antioxidanty (a-tokoferolacetát, kyselina askorbová), hepatoprotektory (essentiale ©, extrakt z artyčoků [hofitol ©]).
· Normalizace procesů excitace a inhibice v centrálním nervovém systému u těhotných žen s astenickou konstitucí a zvýšenou mírou úzkosti. K tomu použijte nootropika (piracetam); glycin, který má významný antistresový účinek.
Adaptogeny (tinktura citronové trávy, eleuterokok, ženšen, aralia) mají dobrý účinek u hypotonické vegetativní vaskulární dystonie.
· K normalizaci spánku používejte složité bylinné přípravky obsahující výtažky z valeriánu, hloh, meduňky, chmele, máty peprné a citronové máty: new-passit ©, léčivé oddenky s kořenovou tinkturou + citronový balzámový bylinkový extrakt + máta peprná, valeriánský léčivé oddenky s kořenovou tinkturou + chmel kužely extrakt.
Léčba a preventivní opatření by měla zahrnovat dietní terapii, vitamínovou terapii, produkty a výživové doplňky, které stimulují funkci střeva (mléčné výrobky, celozrnný chléb, laminolakt).
INFORMACE O PACIENTECH
Placentární nedostatečnost je ohromná komplikace těhotenství, která vede k vysoké morbiditě a úmrtnosti plodu a novorozence. Protože příčinou jejího vývoje jsou nemoci matky (kardiovaskulární onemocnění, onemocnění ledvin, cukrovka), u nichž jsou vývojové mechanismy důležité, jsou cévní poruchy důležité, je proto vhodné při plánování těhotenství tuto patologii prozkoumat a léčit. Výrazně zvyšuje riziko placentární nedostatečnosti u kuřáků, pacientů, kteří požívají alkohol a drogy.
PROGNÓNA PLACENTÁLNÍHO NEDOSTATKU
Příznivé pro mírné hemodynamické poruchy ve funkčním systému matka - placenta - plod.
Pochybné s těžkou podvýživou a těžkou hemodynamickou poruchou.